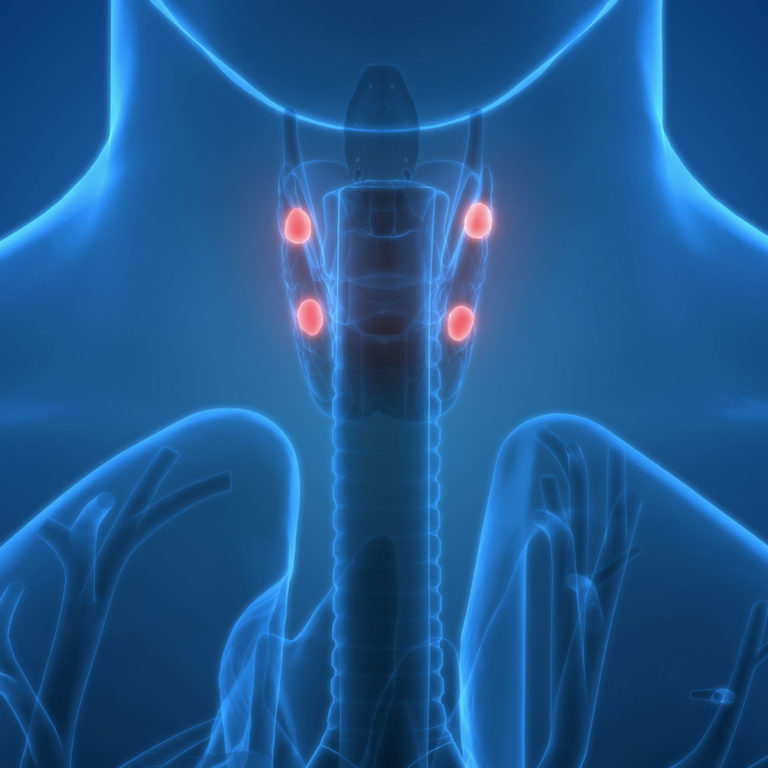
L’approccio diagnostico e terapeutico alle malattie neuromuscolari chiede al clinico di valutare diverse condizioni di malattie che vanno oltre il quadro neuromuscolare specifico che ha portato il paziente all’osservazione del neurologo. Tra gli aspetti extraneurologici sono particolarmente frequenti le alterazioni endocrino-metaboliche, che sono in alcuni casi determinate dalle alterazioni genetiche che causano la malattia neuromuscolare come nelle distrofie miotoniche tipo 1 e tipo 2, in cui frequente e spesso precoce è la comparsa di infertilità e ipogonadismo. Inoltre gli studi più recenti dimostrano che il muscolo è caratterizzato da una funzione endocrina, mediata dal rilascio di miokine, la cui integrità è fondamentale per l’omeostasi di altri metabolismi, come quello osseo e quello glucidico. In questa presentazione si illustrano le acquisizioni più recenti relative a tali aspetti nelle più comuni patologie neuromuscolari.
Ipoparatiroidismo: dalla diagnosi alla terapia
L’ipoparatiroidismo cronico è una condizione caratterizzata da una ridotta o assente secrezione di paratormone, con conseguente ipocalcemia e sintomi ad essa correlati. La terapia si basa sull’assunzione di calcio e forma attiva della vitamina D e, in un prossimo. Futuro, del paratormone umano ricombinante che rappresenta l’ultima terapia sostitutiva delle insufficienze ghiandolari endocrine, in Italia ancora mancante.
Presentiamo una completa disamina della patologia dall’epidemiologia, alla distinzione tra la forma primaria e quella secondaria, per arrivare alla corretta diagnosi. La presentazione di casi clinici aiuta a comprendere come il goal sia quello di mantenere il paziente asintomatico nel tempo con l’impostazione della corretta terapia.
Osso e muscolo: effetti dell’ipovitaminosi D
Approccio multidisciplinare alla gestione del paziente osteoporotico sarcopenico
Iniziare una terapia per le ossa
Quando si riceve un referto di densitometria o si parla per la prima volta di fragilità ossea, una delle domande più frequenti è semplice: devo iniziare una terapia?
La risposta, nella maggior parte dei casi, non è immediata. Non perché manchino indicazioni, ma perché non esiste una regola unica valida per tutti. La decisione di iniziare un trattamento non si basa su un singolo dato, ma su una valutazione più ampia che tiene conto di diversi elementi.
Ed è proprio questo che, per molti pazienti, rende il momento della scelta poco chiaro.
Non conta solo il numero della densitometria
Il valore della MOC è importante, ma da solo non basta a definire cosa fare. Due persone con lo stesso T-score possono avere rischi diversi e quindi indicazioni diverse.
Entrano in gioco l’età, il sesso, la presenza di fratture precedenti, eventuali malattie associate, l’uso di alcuni farmaci e il rischio di caduta. È l’insieme di questi fattori che permette di stimare la probabilità di una frattura nel tempo.
Per questo la decisione non riguarda solo “quanto è basso il numero”, ma cosa significa quel numero in quella persona.
Il ruolo delle fratture
C’è una situazione in cui la decisione diventa più chiara: quando è già avvenuta una frattura da fragilità.
In questi casi, la frattura non è solo un evento passato, ma un segnale concreto di vulnerabilità dello scheletro. E spesso rappresenta un punto di svolta, perché indica che il rischio non è teorico, ma reale.
Per questo motivo, dopo una frattura, la valutazione di una terapia diventa particolarmente importante.
Quando si può scegliere di aspettare
Non sempre iniziare subito una terapia è necessario. In alcune situazioni, soprattutto quando il rischio è basso o intermedio, il medico può proporre un approccio basato su monitoraggio, stile di vita e prevenzione.
Questo non significa “non fare nulla”. Significa lavorare su alimentazione, attività fisica, equilibrio, prevenzione delle cadute e controlli nel tempo. È una scelta attiva, non una rinuncia.
Quando invece aspettare può non essere la scelta migliore
Ci sono però situazioni in cui rimandare può esporre a un rischio maggiore. Quando la densità ossea è molto ridotta, quando sono presenti più fattori di rischio o quando la probabilità di frattura è elevata, iniziare una terapia può rappresentare una forma di protezione.
In questi casi, il trattamento non è un eccesso di cautela, ma un modo per ridurre un rischio concreto. E capire questo aiuta a dare un senso alla proposta terapeutica.
Il peso dei dubbi
Molte persone esitano non perché non comprendano il rischio, ma perché hanno timori legati ai farmaci. È comprensibile. La decisione di iniziare una terapia, soprattutto quando non ci sono sintomi evidenti, può generare incertezza.
Proprio per questo è importante che la scelta non sia subita, ma compresa. Capire perché una terapia viene proposta, quali benefici può offrire e come verrà monitorata permette di affrontarla in modo più consapevole.
Una decisione che si costruisce nel dialogo
Non esiste un momento “giusto” valido per tutti. Esiste un momento giusto per quella persona, in quella fase della sua vita e della sua storia clinica.
Per questo la decisione nasce dal confronto tra paziente e medico. Un confronto in cui è importante portare domande, dubbi, aspettative. Non per mettere in discussione, ma per costruire una scelta condivisa.
Prevenire è diverso da intervenire dopo
C’è un passaggio che spesso fa la differenza: capire che iniziare una terapia non significa solo “curare qualcosa che c’è già”, ma spesso prevenire qualcosa che potrebbe accadere.
Le fratture da fragilità possono avere un impatto importante sulla qualità della vita. Evitarle, quando possibile, è uno degli obiettivi principali.
E questo cambia il modo in cui si guarda al momento della decisione.
Orientarsi senza fretta, ma senza rimandare troppo
Prendersi il tempo per capire è giusto. Ma anche rimandare a lungo una decisione, quando il rischio è elevato, può avere conseguenze.
Trovare un equilibrio tra prudenza e azione è parte del percorso. E spesso, più che cercare una risposta immediata, è utile costruire un ragionamento che permetta di decidere con maggiore serenità.
Ipoparatiroidismo, dalla rarità alla presa in carico
L’ipoparatiroidismo cronico sta entrando in una fase nuova. Non perché la patologia sia diventata improvvisamente più frequente, né perché siano scomparse le difficoltà cliniche che ne caratterizzano la gestione quotidiana. La novità riguarda piuttosto il modo in cui questa condizione rara viene riconosciuta, discussa e collocata all’interno del sistema sanitario: non più soltanto come alterazione del metabolismo calcio-fosforo da correggere sul piano biochimico, ma come malattia endocrinologica sistemica, con un carico clinico e assistenziale che richiede competenze dedicate, continuità di cura e strumenti condivisi.
È questo il messaggio emerso dall’incontro del 28 giugno promosso da A.P.P.I., Associazione per i Pazienti con Ipoparatiroidismo, alla Biblioteca del Senato, in occasione della Giornata Internazionale dell’Ipoparatiroidismo, che si celebra il 1° giugno. Il confronto ha riunito esperti, istituzioni e comunità dei pazienti attorno a tre temi centrali: lo stato della ricerca, l’evoluzione della presa in carico e il riconoscimento dei diritti delle persone che convivono con la patologia.
Secondo le stime richiamate nel corso dell’incontro, l’ipoparatiroidismo interessa circa 10.500 persone in Italia. È un numero contenuto, coerente con la natura rara della malattia, ma sufficiente a porre una questione rilevante per la rete endocrinologica e per i percorsi di cura territoriali e ospedalieri. La rarità, infatti, non riduce la complessità. Al contrario, la amplifica: rende più difficile l’identificazione tempestiva dei casi, accentua la variabilità dei percorsi assistenziali e può esporre i pazienti a ritardi, discontinuità o interpretazioni riduttive dei sintomi.
Una patologia sistemica, non solo una calcemia da correggere
L’ipoparatiroidismo cronico è caratterizzato da una secrezione assente o inadeguata di paratormone, con conseguenti alterazioni del metabolismo del calcio e del fosforo. La forma post-chirurgica, in particolare dopo interventi sulla tiroide o sulle paratiroidi, rappresenta una quota rilevante dei casi, ma non esaurisce lo spettro eziologico della malattia. Alle forme chirurgiche si affiancano forme autoimmuni, genetiche o idiopatiche, nelle quali l’inquadramento diagnostico può richiedere percorsi più articolati.
“L’ipoparatiroidismo è una patologia complessa, sistemica e ancora oggi troppo spesso sottovalutata, che richiede un approccio integrato e multidisciplinare. Negli ultimi anni la ricerca ha compiuto passi importanti, aprendo nuove prospettive terapeutiche e migliorando la comprensione dei meccanismi della malattia – ha affermato Maria Luisa Brandi, Presidente del Comitato Scientifico A.P.P.I. –Tuttavia, è fondamentale continuare a investire nella conoscenza e nella diffusione di competenze, affinché queste innovazioni si traducano concretamente in una migliore qualità della cura”.
Per lo specialista, difatti, il punto critico non è soltanto riportare la calcemia in un intervallo accettabile. La gestione dell’ipoparatiroidismo implica il controllo dell’equilibrio calcio-fosforo, la prevenzione dell’ipercalciuria, la sorveglianza della funzione renale, l’attenzione al rischio di calcificazioni ectopiche e la valutazione del burden sintomatologico. Parestesie, crampi, affaticabilità, disturbi cognitivi, manifestazioni neuropsichiche e riduzione della qualità di vita possono persistere anche in presenza di parametri apparentemente controllati, ponendo un problema di appropriatezza del follow-up e di reale personalizzazione terapeutica.
È in questa prospettiva che l’affermazione di Maria Luisa Brandi, Presidente del Comitato Scientifico A.P.P.I., assume un significato clinico preciso: l’ipoparatiroidismo è una patologia complessa, sistemica e ancora sottovalutata, che richiede un approccio integrato e multidisciplinare. La ricerca ha compiuto progressi importanti, ma il passaggio decisivo resta la traduzione dell’innovazione in una migliore qualità della cura.
La nuova stagione terapeutica
Per molti anni, la terapia convenzionale dell’ipoparatiroidismo cronico si è basata sulla supplementazione con calcio e vitamina D attiva, con l’obiettivo di controllare l’ipocalcemia e ridurre i sintomi. Questo approccio resta centrale e continua a rappresentare il trattamento di riferimento per molti pazienti. Tuttavia, la terapia convenzionale non sostituisce la funzione endocrina del paratormone e può risultare insufficiente in una quota di casi, soprattutto quando il controllo biochimico è instabile, il carico di supplementazione elevato, l’ipercalciuria difficile da gestire o la qualità di vita significativamente compromessa.
L’arrivo delle terapie sostitutive con PTH modifica il quadro clinico e apre una prospettiva diversa: trattare non soltanto le conseguenze biochimiche della carenza ormonale, ma almeno in parte il deficit endocrino alla base della malattia. In Europa, palopegteriparatide ha ricevuto l’autorizzazione come terapia sostitutiva dell’ormone paratiroideo per adulti con ipoparatiroidismo cronico. In Italia, la disponibilità in regime di rimborsabilità SSN è stata attivata attraverso il registro AIFA per pazienti adulti non adeguatamente controllati con terapia convenzionale e secondo specifici criteri di eleggibilità e appropriatezza.
Per gli specialisti, questo passaggio non va letto come una semplice aggiunta farmacologica. Richiede una selezione accurata dei pazienti, un monitoraggio strutturato, una valutazione del rapporto beneficio-rischio e una particolare attenzione alla transizione terapeutica. Le più recenti linee guida europee sottolineano che la terapia sostitutiva con PTH può ridurre il carico della terapia convenzionale e migliorare diversi parametri biochimici, ma richiede competenza nella gestione clinica e prudenza nella valutazione degli esiti di lungo periodo, ancora oggetto di approfondimento.
La questione centrale, quindi, non è sostituire un modello terapeutico con un altro, ma definire quali pazienti possano beneficiare di una strategia più fisiologica e in quali condizioni organizzative questa strategia possa essere applicata in modo sicuro, sostenibile e omogeneo.
Dalla disponibilità terapeutica all’accesso reale
L’innovazione terapeutica, da sola, non garantisce equità di cura. Nell’ipoparatiroidismo cronico, il rischio di disomogeneità è particolarmente elevato, perché la patologia si colloca all’incrocio tra endocrinologia, chirurgia, medicina interna, nefrologia, medicina generale e, non di rado, ambiti amministrativi complessi legati a esenzioni, invalidità, tutele lavorative e riconoscimento del carico assistenziale.
Per questo il confronto promosso da A.P.P.I. ha affiancato al tema della ricerca quello dei diritti e dell’orientamento dei pazienti. Il Progetto Pazienti “Le Linee Guida Italiane” è stato presentato come uno strumento per favorire una gestione più uniforme e consapevole della patologia sul territorio nazionale. Non si tratta soltanto di divulgare informazioni, ma di ridurre la distanza tra sapere specialistico, percorsi regionali e vissuto quotidiano delle persone.
In parallelo, la “Guida ai diritti dei pazienti con ipoparatiroidismo” risponde a un bisogno spesso trascurato nella pratica clinica: aiutare pazienti e caregiver a orientarsi tra normative, esenzioni e tutele. Per una condizione cronica, potenzialmente invalidante e ancora poco riconosciuta, la dimensione dei diritti non è accessoria. È parte della presa in carico, perché incide sulla continuità delle cure, sull’aderenza ai percorsi, sulla possibilità di accedere a centri competenti e sulla capacità del paziente di partecipare in modo informato alle decisioni terapeutiche.
Come ha evidenziato Marta Cecconi, Presidente A.P.P.I., molti pazienti affrontano percorsi complessi, frammentati e poco chiari. L’obiettivo dell’associazione è contribuire a colmare questo divario con strumenti accessibili, costruiti a partire dall’esperienza diretta delle persone, e favorire un dialogo più efficace con il sistema sanitario.
Il ruolo dello specialista in una rete più consapevole
Per la comunità clinica, l’emersione dell’ipoparatiroidismo nel dibattito sanitario rappresenta un’opportunità e una responsabilità. L’opportunità è quella di migliorare la capacità di identificazione, stratificazione e follow-up dei pazienti. La responsabilità riguarda invece la costruzione di percorsi che non si limitino al controllo episodico degli esami, ma integrino monitoraggio metabolico, valutazione renale, burden sintomatologico, qualità di vita e appropriatezza terapeutica.
In questa prospettiva, alcuni elementi appaiono prioritari: riconoscere precocemente le forme croniche dopo chirurgia cervicale; distinguere i pazienti ben controllati da quelli con controllo insufficiente o instabile; monitorare il rischio renale e l’ipercalciuria; valutare il carico complessivo della terapia convenzionale; indirizzare i casi complessi verso centri con esperienza specifica; integrare le nuove opzioni terapeutiche all’interno di criteri condivisi e verificabili.
La disponibilità di strumenti informativi per i pazienti può favorire questo processo, ma non può sostituire la governance clinica. Al contrario, rende ancora più importante il ruolo dello specialista come garante dell’appropriatezza, dell’interpretazione dei dati e della continuità decisionale. Un paziente più informato non riduce la complessità del percorso: la rende più esplicita e richiede un’interlocuzione clinica più matura.
Una malattia rara che chiede percorsi riconoscibili
L’ipoparatiroidismo cronico resta una patologia rara, ma il suo impatto non è marginale. Interessa la qualità di vita, la funzione renale, l’equilibrio metabolico, la vita lavorativa e la relazione del paziente con il sistema sanitario. La nuova fase aperta dalla ricerca e dalle terapie sostitutive con PTH impone di superare una visione puramente correttiva della malattia e di costruire percorsi più riconoscibili, misurabili e omogenei.
Il confronto promosso da A.P.P.I. indica una direzione precisa: portare l’ipoparatiroidismo fuori da una zona grigia fatta di bassa consapevolezza, frammentazione assistenziale e riconoscimento incompleto. Per gli specialisti, questo significa contribuire a trasformare l’innovazione disponibile in pratica clinica appropriata. Per il sistema sanitario, significa garantire che rarità non diventi sinonimo di invisibilità.
La posta in gioco non è soltanto l’accesso a una nuova opzione terapeutica. È la possibilità di riconoscere l’ipoparatiroidismo cronico come una condizione endocrinologica complessa, da seguire con competenze dedicate, strumenti condivisi e una presa in carico realmente orientata agli esiti che contano per il paziente.
Quando chiedere un secondo parere
Quando si riceve una diagnosi o viene proposta una terapia, soprattutto se riguarda una condizione cronica come l’osteoporosi o una fragilità ossea, è normale avere domande. Non sempre, però, è facile esprimerle. Si tende a fidarsi, a rimandare, oppure a cercare risposte altrove, spesso in modo poco strutturato.
In questo contesto nasce il pensiero del secondo parere. A volte come esigenza chiara, altre come dubbio che resta sullo sfondo: “E se sentissi un altro medico?”
Non è una domanda sbagliata. Ma è una domanda che va collocata nel modo giusto.
Non è una sfiducia, ma una ricerca di chiarezza
Chiedere un secondo parere viene talvolta percepito come un gesto di diffidenza nei confronti del medico. In realtà, nella maggior parte dei casi, nasce da un bisogno diverso: capire meglio.
Quando una situazione è complessa, quando le opzioni terapeutiche non sono immediate, quando i benefici e i possibili effetti collaterali devono essere valutati con attenzione, ascoltare un’altra opinione può aiutare a mettere a fuoco il quadro. Non per “mettere in discussione”, ma per comprendere.
Quando può essere davvero utile
Non tutte le situazioni richiedono un secondo parere. In molti casi, il percorso è chiaro e condiviso, e aggiungere un altro passaggio non porta un reale beneficio.
Ci sono però momenti in cui può avere senso fermarsi e chiedere un confronto.
Quando la diagnosi non è del tutto chiara, quando le opzioni terapeutiche sono diverse e non esiste una scelta unica, quando una terapia proposta genera dubbi o timori difficili da sciogliere, oppure quando il problema non migliora come previsto. Sono situazioni in cui una seconda valutazione può offrire un punto di vista complementare.
Quando invece rischia di creare confusione
Esiste anche il rischio opposto: quello di moltiplicare i pareri senza riuscire a integrarli. Consultare molti specialisti senza un coordinamento può portare a indicazioni diverse, talvolta contrastanti, che invece di chiarire rendono più difficile decidere.
In questi casi il problema non è il secondo parere in sé, ma il modo in cui viene cercato. Un confronto mirato è diverso da una ricerca continua di conferme.
Come chiedere un secondo parere in modo utile
Se si decide di farlo, è importante farlo bene.
Portare con sé tutta la documentazione disponibile, spiegare chiaramente la propria situazione, condividere la diagnosi ricevuta e la terapia proposta. Non partire da zero, ma costruire su quanto già fatto.
Questo permette allo specialista di dare un contributo reale, e non una valutazione parziale. E, se possibile, mantenere un collegamento con il medico di riferimento aiuta a integrare le informazioni, invece di sovrapporle.
Il ruolo del medico di riferimento
In questo percorso, il medico di base o lo specialista che segue il caso può avere un ruolo importante.
Non come figura da “sostituire”, ma come punto di riferimento che aiuta a interpretare i diversi pareri e a costruire una sintesi. È una figura che conosce il contesto, la storia clinica, le priorità della persona. E questo, quando si devono prendere decisioni, conta.
Un equilibrio tra fiducia e consapevolezza
Alla base di tutto c’è un equilibrio delicato. Da una parte la fiducia nel medico, che è essenziale per costruire un percorso di cura. Dall’altra il bisogno di comprendere e partecipare alle decisioni.
Il secondo parere, quando è usato nel modo giusto, non rompe questo equilibrio. Può rafforzarlo. Perché permette di arrivare a una scelta più consapevole.
Decidere con maggiore serenità
In molti casi, ciò che il paziente cerca non è tanto una risposta diversa, ma una maggiore sicurezza nella decisione da prendere.
Avere ascoltato un altro punto di vista può aiutare proprio in questo: ridurre il dubbio, chiarire le priorità, comprendere meglio i pro e i contro.
Non sempre cambia la direzione della terapia. Ma spesso cambia il modo in cui la si affronta.
Acromegalia, qualità di vita e danno osseo
L’acromegalia è tradizionalmente descritta come una malattia endocrina rara causata, nella maggior parte dei casi, da un adenoma ipofisario secernente GH, con conseguente incremento dei livelli di IGF-I. È però riduttivo leggerla soltanto attraverso la lente biochimica. L’eccesso cronico di GH e IGF-I produce un coinvolgimento multisistemico progressivo, che interessa metabolismo, apparato cardiovascolare, respirazione notturna, funzione neuropsicologica, apparato muscoloscheletrico e percezione corporea. La review di Eliza B. Geer e Jill Sisco, pubblicata su The Journal of Clinical Endocrinology & Metabolism, parte proprio da questo punto: il controllo biochimico migliora gli outcome, ma molti pazienti continuano a riferire sintomi persistenti, ridotta qualità di vita e un carico terapeutico non trascurabile.
Il tema è particolarmente rilevante per lo specialista del metabolismo osseo perché una quota importante del burden dell’acromegalia passa attraverso dolore articolare, artropatia, alterazioni della performance fisica, aumentato rischio di osteoporosi e fratture vertebrali. Non si tratta di manifestazioni accessorie, ma di determinanti centrali della disabilità residua, anche quando la malattia viene considerata “controllata” sul piano ormonale.
La remissione funzionale come nuovo obiettivo clinico
Nella pratica clinica, il successo terapeutico dell’acromegalia viene spesso definito attraverso tre obiettivi principali: normalizzazione di IGF-I, controllo della secrezione di GH, riduzione o stabilizzazione del volume tumorale. Sono parametri indispensabili, ma non esauriscono l’esperienza di malattia. Gli autori sottolineano che i pazienti tendono a considerare prioritario un obiettivo più ampio, definibile come remissione funzionale: recuperare autonomia, ruolo sociale, capacità lavorativa, benessere psicologico e una quotidianità meno condizionata dai sintomi.
Il punto critico è la discordanza tra stato biochimico e percezione clinica. La severità dei sintomi non correla sempre con i livelli di GH e IGF-I; inoltre, la valutazione del paziente può divergere sensibilmente da quella del medico. Da qui deriva l’importanza dei patient-reported outcomes, cioè strumenti che raccolgono direttamente dal paziente informazioni su sintomi, qualità di vita, funzione e impatto del trattamento, senza mediazione interpretativa del clinico.
Tra gli strumenti specifici per l’acromegalia, la review richiama l’Acromegaly Quality of Life Questionnaire, il Patient-Assessed Acromegaly Symptom Questionnaire, l’Acromegaly Treatment Satisfaction Questionnaire e l’Acromegaly Symptom Diary. Quest’ultimo è particolarmente interessante perché consente una valutazione giornaliera dei sintomi, intercettando fluttuazioni che possono sfuggire alla visita periodica.
Sintomi fisici persistenti e burden muscoloscheletrico
Fatigue, debolezza muscolare e dolore articolare sono tra i sintomi più disturbanti riferiti dai pazienti con acromegalia. La review riporta che questi disturbi interessano il 79-92% dei pazienti e impattano direttamente sulla funzionalità quotidiana. Anche le modificazioni acrali e dei tessuti molli sono molto frequenti alla diagnosi, mentre iperidrosi, apnea ostruttiva del sonno, sindrome del tunnel carpale e cefalea contribuiscono ulteriormente al quadro clinico.
Il coinvolgimento muscoloscheletrico è uno dei capitoli più rilevanti. Le condizioni muscoloscheletriche interessano oltre l’80% dei pazienti e contribuiscono a riduzione della qualità di vita, disabilità e maggiore utilizzo di risorse sanitarie. L’artropatia, presente in circa il 70% dei pazienti alla diagnosi, può associarsi ad artrite poliarticolare, osteofitosi e fratture vertebrali, con dolore invalidante e limitazione funzionale.
Un dato importante riguarda la storia naturale del danno articolare. In uno studio di registro danese citato dagli autori, 844 pazienti con acromegalia sono stati confrontati con controlli sani, mostrando un aumento del rischio di osteoartrosi di spalla e ginocchio già prima della diagnosi, oltre a un incremento degli interventi di sostituzione articolare e delle complicanze postoperatorie. Ancora più significativo, l’osteoartrosi tendeva a progredire nel tempo anche dopo il trattamento della malattia endocrina.
Questa osservazione ha implicazioni cliniche dirette: il controllo biochimico non sempre arresta il danno strutturale già instaurato. L’artropatia acromegalica, una volta consolidata, può diventare scarsamente reversibile. La persistenza del dolore articolare e delle limitazioni motorie va quindi interpretata non come semplice “residuo soggettivo”, ma come espressione di un danno organico che richiede valutazione e gestione specifica.
Osso, microarchitettura e fratture vertebrali
La review dedica un passaggio rilevante anche al metabolismo osseo. L’acromegalia è associata a una forma di osteoporosi ad alto turnover, caratterizzata da compromissione della microarchitettura scheletrica e aumentato rischio di fratture vertebrali, spesso in presenza di densità minerale ossea normale.
Nel paziente acromegalico, la BMD può non riflettere pienamente la fragilità scheletrica. Il rischio vertebrale dipende da alterazioni qualitative dell’osso, dalla durata dell’esposizione a GH/IGF-I, dall’eventuale ipogonadismo e dalle comorbidità. L’ipogonadismo, presente in almeno il 20% dei pazienti secondo la review, aggrava ulteriormente il rischio fratturativo.
Ne deriva la necessità di una valutazione più fine del rischio scheletrico. Nel paziente con acromegalia, soprattutto se la diagnosi è stata tardiva, la sola densitometria può essere insufficiente. L’attenzione alle fratture vertebrali morfometriche, alla qualità ossea, alla storia clinica e alla funzione gonadica diventa parte integrante del follow-up. In questa prospettiva, lo specialista del metabolismo osseo ha un ruolo non marginale nella presa in carico multidisciplinare.
Il peso del ritardo diagnostico
Uno dei determinanti principali del burden clinico è il ritardo diagnostico. La progressione dei sintomi fisici avviene nel tempo, sotto l’effetto prolungato dell’eccesso di GH e IGF-I. Gli autori ricordano che la durata della malattia non trattata contribuisce alla severità del quadro e che l’artropatia può persistere anche dopo il raggiungimento del controllo biochimico.
Il ritardo diagnostico ha anche una dimensione di genere. Le donne, secondo la review, possono arrivare alla diagnosi più tardi rispetto agli uomini, con una differenza riportata tra 2 e 4,6 anni, e tendono a presentare più comorbidità, peggiore funzionamento fisico e qualità di vita più compromessa.
Per lo specialista, questo dato richiama l’importanza di intercettare pattern clinici apparentemente dispersi: artropatia precoce o atipica, incremento delle dimensioni acrali, cefalea, tunnel carpale, apnea notturna, alterazioni metaboliche, fratture vertebrali non spiegate dalla BMD. La diagnosi precoce resta il primo intervento capace di modificare la traiettoria del danno.
Qualità di vita, depressione e immagine corporea
La compromissione della qualità di vita nell’acromegalia coinvolge domini fisici, psicologici e sociali. La review riporta che alla diagnosi i punteggi AcroQoL sono generalmente ridotti, con valori pari a circa il 57-69% dei valori normativi. I disturbi dell’umore sono frequenti: la depressione interessa circa il 28-35% dei pazienti, mentre sintomi ansiosi possono essere riportati fino al 66%.
Il dato più interessante è che la qualità di vita può rimanere compromessa anche dopo anni di controllo biochimico. In studi longitudinali citati dagli autori, una quota consistente di pazienti mantiene punteggi inferiori alla norma in diversi domini dell’SF-36 anche dopo 15-20 anni di controllo stabile. L’area dell’aspetto fisico e dell’autostima risulta tra le più colpite, a conferma dell’impatto delle modificazioni somatiche sulla vita psicologica e relazionale.
Anche in questo caso, il messaggio clinico è netto: la normalizzazione ormonale non coincide automaticamente con il recupero soggettivo. Il paziente può essere “controllato” nei parametri e tuttavia continuare a vivere dolore, fatigue, limitazioni funzionali, disagio corporeo, ansia sociale e ridotta partecipazione lavorativa.
Trattamenti, burden terapeutico e sintomi breakthrough
Le terapie dell’acromegalia migliorano sintomi e qualità di vita, ma il beneficio dipende da efficacia biochimica, reversibilità del danno e tollerabilità. La chirurgia transsfenoidale può offrire miglioramenti importanti, soprattutto se consente la remissione. La radioterapia, invece, può richiedere anni per ottenere il controllo biochimico e può associarsi a ipopituitarismo, con ulteriore impatto sul benessere del paziente.
La terapia medica presenta un quadro più complesso. Nei pazienti trattati con analoghi della somatostatina iniettabili, una quota significativa continua a riferire sintomi persistenti. La review cita dati secondo cui due terzi dei pazienti biochimicamente controllati in trattamento con SRL continuavano a presentare sintomi di acromegalia, con l’82% che li riferiva “sempre”. Fatigue, debolezza muscolare, dolore articolare, tumefazione dei tessuti molli, cefalea e iperidrosi restano quindi problemi clinici aperti.
Un ulteriore elemento è il burden del trattamento. Iniezioni ripetute, dolore locale, reazioni al sito di somministrazione, vincoli logistici, sintomi gastrointestinali e possibile ricomparsa di sintomi verso la fine del ciclo terapeutico possono interferire con vita quotidiana, lavoro e aderenza.
Le formulazioni orali e le nuove opzioni terapeutiche potrebbero ridurre parte di questo carico, migliorando autonomia e soddisfazione del paziente. Tuttavia, gli autori sottolineano che i dati comparativi sui patient-reported outcomes restano ancora limitati e che servono studi head-to-head più robusti.
Verso una presa in carico realmente multidisciplinare
La review propone un cambio di prospettiva clinica: il successo terapeutico nell’acromegalia dovrebbe essere definito come controllo biochimico più recupero della qualità di vita. Questo richiede una valutazione sistematica di sintomi, funzione fisica, salute mentale, soddisfazione terapeutica, produttività lavorativa e burden economico.
La presa in carico ottimale include endocrinologo, neurochirurgo, neuroradiologo, radioterapista, cardiologo, specialista del sonno, gastroenterologo, neuro-oftalmologo e professionisti della salute mentale. A questa rete va aggiunto, in modo esplicito, lo specialista del metabolismo osseo, soprattutto nei pazienti con dolore muscoloscheletrico persistente, artropatia, ipogonadismo, sospetto di fragilità vertebrale o discrepanza tra BMD e quadro clinico.
La lezione più importante dello studio è che l’acromegalia non può essere seguita solo attraverso il laboratorio. GH e IGF-I restano indicatori fondamentali, ma non raccontano da soli la storia clinica del paziente. Dolore, fatigue, mobilità, rischio fratturativo, immagine corporea e vita sociale sono outcome clinici a pieno titolo.
Per questo, l’integrazione dei PRO nella pratica endocrinologica e nei trial clinici non va considerata un’aggiunta “umanistica”, ma una necessità metodologica. Solo misurando ciò che il paziente continua a vivere dopo la remissione biochimica sarà possibile distinguere il controllo della malattia dal recupero della persona.
Fonte
Eliza B Geer, Jill Sisco, The Acromegaly Patient Experience: Burden of Treatment, Breakthrough Symptoms, and Quality of Life, The Journal of Clinical Endocrinology & Metabolism, 2026; dgag122.
Chi si occupa delle ossa?
Davanti a un problema che riguarda le ossa, la prima difficoltà non è sempre il sintomo, ma capire a chi rivolgersi. Dolore alla schiena, una frattura, un referto di densitometria non chiaro: situazioni diverse che spesso portano alla stessa domanda.
Serve un ortopedico? Un endocrinologo? Un reumatologo? Oppure basta parlarne con il medico di base?
Non è una domanda banale, perché le patologie dell’osso non appartengono a una sola specialità. Sono un terreno condiviso, in cui competenze diverse si incontrano. Ed è proprio questo che, per chi non è del settore, può generare confusione.
Il medico di base: il primo punto di riferimento
Nella maggior parte dei casi, il primo passo resta il medico di medicina generale. Non solo perché è il punto di accesso più immediato, ma perché conosce la storia clinica della persona, i fattori di rischio, le eventuali altre patologie.
È spesso il medico di base a intercettare un sospetto di fragilità ossea, a consigliare una densitometria o a indirizzare verso uno specialista. Il suo ruolo non è sostituire gli altri professionisti, ma aiutare a orientare il percorso. E questo, soprattutto all’inizio, fa una grande differenza.
L’ortopedico: quando il problema è strutturale
L’ortopedico è lo specialista a cui si pensa più facilmente quando si parla di ossa. Ed è corretto, soprattutto quando il problema riguarda una frattura, un trauma, una deformità o una condizione che coinvolge direttamente la struttura dell’apparato muscolo-scheletrico.
È la figura di riferimento nelle fasi acute, per esempio dopo una caduta o quando si rende necessario un intervento chirurgico. Ma può essere coinvolto anche nella gestione di condizioni croniche che hanno una componente meccanica o strutturale.
L’endocrinologo: quando entra in gioco il metabolismo
Non tutte le malattie dell’osso sono legate a traumi o a problemi meccanici. Molte dipendono dal modo in cui l’organismo regola il metabolismo osseo.
L’endocrinologo si occupa proprio di questo: del ruolo degli ormoni, del metabolismo del calcio, delle condizioni che possono influenzare la densità e la qualità dell’osso. È una figura centrale nella gestione dell’osteoporosi e di molte altre condizioni metaboliche.
Quando si parla di fragilità ossea senza un trauma evidente, spesso è questo lo specialista di riferimento.
Il reumatologo: quando l’infiammazione ha un ruolo
Ci sono situazioni in cui il problema dell’osso è legato a malattie infiammatorie o autoimmuni. In questi casi entra in gioco il reumatologo.
Artrite reumatoide, connettiviti, malattie infiammatorie croniche possono influenzare anche la salute delle ossa. Il reumatologo ha una visione che integra articolazioni, sistema immunitario e tessuto osseo.
Non è sempre il primo specialista a cui si pensa, ma in alcune condizioni è fondamentale.
Il fisiatra e il fisioterapista: quando il problema è il movimento
C’è un altro aspetto che spesso viene sottovalutato: la funzione.
Dolore, rigidità, perdita di equilibrio, difficoltà nel movimento sono elementi che non riguardano solo la diagnosi, ma la qualità della vita. In questi casi il fisiatra e il fisioterapista hanno un ruolo centrale.
Lavorano sul recupero, sulla prevenzione delle cadute, sulla postura, sulla sicurezza nei movimenti. E questo, soprattutto nelle persone con fragilità ossea, è parte integrante della cura.
Non è una scelta “uno o l’altro”
Un errore comune è pensare che si debba scegliere uno specialista “giusto” e che gli altri siano alternativi. In realtà, molto spesso il percorso migliore è integrato.
Un paziente può essere seguito dal medico di base, valutato da uno specialista per la diagnosi e affiancato da professionisti della riabilitazione per la parte funzionale.
Non è una complicazione. È una presa in carico più completa.
Orientarsi è già parte della cura
Se il dubbio resta, il punto non è indovinare lo specialista giusto da soli. È chiedere.
Parlare con il medico di base, portare gli esami, spiegare i sintomi, chiarire cosa non è chiaro. Da lì il percorso si costruisce. E spesso, una volta fatto il primo passo, diventa molto più lineare di quanto si pensi.
Capire a chi rivolgersi, infatti, non è solo una questione organizzativa. È il primo passo per affrontare un problema nel modo giusto.
Perché arrivare allo specialista più adatto, nel momento giusto, significa evitare passaggi inutili, ridurre i tempi e, soprattutto, sentirsi meno soli davanti a qualcosa che non si conosce.
E, in molti casi, è proprio questo che cambia l’esperienza del paziente.
Quando il muscolo protegge anche l’osso
Quando si parla di fragilità scheletrica, l’attenzione si concentra quasi sempre sull’osso. Si parla di densità minerale, di osteoporosi, di rischio di frattura. È naturale che sia così, ma questa visione rischia di essere incompleta.
Le ossa non lavorano isolate. Fanno parte di un sistema in cui il muscolo ha un ruolo fondamentale. Sostiene il movimento, contribuisce all’equilibrio, protegge dalle cadute e, in modo meno intuitivo ma altrettanto importante, partecipa alla salute stessa dello scheletro.
Negli ultimi anni si è capito sempre meglio che, per comprendere davvero il rischio di fragilità, non basta guardare all’osso. Bisogna guardare anche a ciò che accade al muscolo. Ed è qui che entra in gioco la sarcopenia.
Cos’è davvero la sarcopenia
Il termine può sembrare tecnico, ma il fenomeno è concreto e riguarda molte persone, spesso senza che ne siano consapevoli. La sarcopenia è una progressiva riduzione di massa muscolare, forza e funzione fisica.
Non significa semplicemente sentirsi un po’ più deboli. Significa che il sistema che aiuta il corpo a mantenersi stabile, reagire, sostenersi e muoversi con sicurezza perde efficienza.
Questo processo può accompagnare l’età, ma non va considerato una conseguenza inevitabile dell’invecchiamento. Può essere favorito dalla sedentarietà, da malattie croniche, da periodi di immobilità, da ricoveri o da recuperi difficili dopo una frattura.
E proprio per questo riconoscerlo conta.
Perché riguarda anche la salute delle ossa
Pensare a muscolo e osso come due sistemi separati è un errore sempre meno sostenibile. Il loro rapporto è molto stretto.
I muscoli proteggono lo scheletro non solo perché aiutano a evitare cadute, ma anche perché il movimento e il carico meccanico contribuiscono a mantenere l’osso stimolato e attivo.
Quando la funzione muscolare si riduce, non cambia soltanto la forza. Può cambiare la stabilità, la postura, la sicurezza nei movimenti. E questo può tradursi in un aumento del rischio di eventi che mettono a rischio anche l’osso.
Per questo oggi si parla sempre più spesso di asse muscolo-osso, e non come formula teorica, ma come chiave concreta per capire la fragilità.
Un problema che spesso si nota tardi
Uno degli aspetti più insidiosi della sarcopenia è che tende a progredire lentamente. Non si manifesta come un evento improvviso. Più spesso si insinua con piccoli cambiamenti che sembrano quasi normali.
Ci si alza con più fatica da una sedia. Si cammina più lentamente. Si evita una scala che prima non creava problemi. Ci si sente meno sicuri nei movimenti.
Presi singolarmente, questi segnali possono sembrare irrilevanti. Ma nel loro insieme possono raccontare qualcosa. Ed è proprio perché questi cambiamenti possono apparire “normali” che spesso vengono sottovalutati.
Quando si incontra con l’osteoporosi
C’è una combinazione che merita particolare attenzione: quella tra fragilità ossea e perdita di funzione muscolare.
Quando queste due condizioni si sommano, il rischio può aumentare non solo perché l’osso è più vulnerabile, ma perché la probabilità di cadere può diventare maggiore.
È un aspetto molto importante, perché sposta l’attenzione da una visione centrata solo sullo scheletro a una visione più completa della prevenzione. Proteggere l’osso, in molti casi, significa anche proteggere il movimento.
Si può fare qualcosa?
Sì, ed è una parte molto importante del messaggio. La sarcopenia non è necessariamente un processo da subire passivamente.
L’attività fisica mirata ha un ruolo centrale. In particolare il lavoro su forza, equilibrio e funzione può contribuire in modo significativo a mantenere autonomia e ridurre vulnerabilità.
Anche l’alimentazione ha un ruolo importante, soprattutto quando ci sono carenze, ridotto apporto proteico o condizioni che favoriscono perdita muscolare.
Spesso non si tratta di interventi straordinari, ma di riconoscere il problema in tempo e affrontarlo prima che la perdita di funzione diventi rilevante.
Un cambio di prospettiva che può fare la differenza
Per anni la prevenzione delle fratture è stata pensata soprattutto intorno all’osso.
Oggi si capisce sempre meglio che questa visione, da sola, non basta.
Bisogna guardare anche alla forza, all’equilibrio, alla qualità del movimento. Bisogna guardare al muscolo.
E questo non è un dettaglio tecnico. È un cambio di prospettiva. Perché capire che proteggere il muscolo significa, spesso, proteggere anche l’osso, cambia il modo di pensare alla fragilità.
E può cambiare anche il modo di prevenirla.
Acromegalia, nuove terapie e nuovi target
Per decenni, il trattamento dell’acromegalia si è mosso lungo una traiettoria relativamente stabile: chirurgia ipofisaria, analoghi della somatostatina, antagonismo recettoriale e, nei casi selezionati, radioterapia. Un modello efficace, ma non privo di limiti. Non tutti i pazienti raggiungono un controllo biochimico ottimale; molti convivono con sintomi persistenti nonostante valori apparentemente normalizzati di IGF-I; altri pagano un prezzo elevato in termini di burden terapeutico, soprattutto per la dipendenza da terapie iniettive croniche.
È dentro queste criticità che si inserisce la nuova generazione di terapie oggi in sviluppo o recentemente approvate. Ma la novità non riguarda soltanto molecole e formulazioni. Riguarda il modo stesso di leggere la malattia.
Sta emergendo infatti un cambiamento concettuale importante: il controllo dell’acromegalia potrebbe non coincidere più, in futuro, con la sola normalizzazione dell’IGF-I circolante.
Il nodo irrisolto del controllo “incompleto”
Nella pratica clinica, il paradosso è noto. Pazienti biochimicamente controllati possono continuare a presentare artropatia, alterazioni metaboliche, dolore, fatigue o ridotta qualità di vita.
Il problema, suggerisce la letteratura più recente, è che l’IGF-I potrebbe non catturare integralmente l’attività patologica residua del GH.
Da qui prende forza il concetto di acromegalia extraepatica: una condizione in cui, pur con apparente controllo epatico e normalizzazione dell’IGF-I, può persistere un’eccessiva attività del GH a livello periferico — in osso, cartilagine, muscolo, rene e tessuto adiposo.
Per chi si occupa di metabolismo osseo, il punto è tutt’altro che marginale. L’asse GH/IGF-I non agisce solo come regolatore endocrino sistemico, ma come modulatore diretto del turnover scheletrico, della cartilagine e della biomeccanica ossea.
Questo rende plausibile che il futuro della terapia non passi solo da farmaci più comodi, ma da strategie capaci di distinguere e trattare componenti diverse della malattia.
Analoghi della somatostatina, verso una nuova generazione
Una prima direttrice di innovazione riguarda il perfezionamento delle terapie consolidate.
Tra le novità più avanzate vi è CAM2029, formulazione sottocutanea depot di octreotide approvata in Europa nel 2025. Nello studio ACROINNOVA-1 ha mostrato mantenimento del controllo biochimico nel 72,2% dei pazienti, con miglioramenti anche su qualità di vita e soddisfazione terapeutica.
Il dato interessante non è solo l’efficacia. È il tentativo di spostare il focus da “funzionare” a “funzionare con minore peso terapeutico”.
Una logica che si ritrova anche in Debio 4126, formulazione di octreotide a somministrazione trimestrale. Se confermata negli studi di fase 3, potrebbe ridurre radicalmente la frequenza delle iniezioni, modificando in modo concreto la gestione cronica.
Parallelamente, gli agonisti orali come paltusotine introducono un’altra rottura: portare una parte della terapia fuori dalla logica iniettiva. Non è un dettaglio organizzativo. È un possibile cambio di paradigma.
Il recettore del GH come nuovo bersaglio
La seconda linea di innovazione è ancora più interessante. Non agire più solo a monte, bloccando la secrezione ipofisaria di GH, ma a valle, interferendo direttamente con il suo segnale biologico. Qui si collocano i nuovi antagonisti del recettore del GH.
ALXN2420, peptide biciclico in sviluppo clinico, punta a rafforzare l’approccio inaugurato da pegvisomant, ma con un profilo farmacologico nuovo e potenziale uso add-on con analoghi della somatostatina. I dati preliminari mostrano riduzione dose-dipendente dell’IGF-I e possibili effetti additivi in combinazione.
Ancora più innovativo è MAR002, anticorpo monoclonale allosterico che non compete con GH sul sito di legame, ma ne impedisce l’attivazione recettoriale attraverso un meccanismo diverso.
L’interesse scientifico è enorme: non si tratta semplicemente di avere un altro antagonista. Si apre la possibilità di modulare il segnale GH con logiche farmacologiche completamente nuove.
Cosa cambia per l’osso
Per il metabolismo osseo, questa evoluzione merita attenzione particolare.
L’acromegalia è una patologia in cui densità minerale, microarchitettura e rischio fratturativo non seguono sempre relazioni intuitive. La discrepanza tra BMD apparentemente conservata e fragilità vertebrale è ben documentata.
Se parte di questa complessità dipende da attività periferica GH-mediata non intercettata dall’IGF-I, allora le terapie che modulano anche la componente extraepatica potrebbero avere implicazioni che vanno oltre il controllo endocrino.
Non è ancora dimostrato che questi nuovi farmaci migliorino direttamente outcome scheletrici. Ma la domanda è ormai aperta. Ed è probabilmente una delle più interessanti per la ricerca futura.
Verso una medicina più personalizzata
Il messaggio forse più forte che emerge non riguarda una singola molecola. Riguarda la fine di un approccio unico per tutti.
Profilo tumorale, burden sintomatologico, comorbidità metaboliche, caratteristiche del recettore, possibile dissociazione tra controllo biochimico e clinico: tutto spinge verso una terapia più stratificata.
In questo scenario, combinare soppressione adenoma-diretta e modulazione periferica del GH potrebbe diventare, in molti casi, non un’eccezione, ma una strategia ordinaria.
È un cambiamento profondo. Perché ridefinisce il concetto stesso di controllo.
Il futuro non è solo avere più farmaci
Per anni l’innovazione in acromegalia è stata misurata in nuove molecole.
Oggi il parametro sembra diverso. Conta sempre più come il farmaco agisce, quanto riduce il carico terapeutico, se controlla davvero la malattia, e se migliora sintomi, funzione, qualità di vita.
In questo senso, il futuro dell’acromegalia potrebbe non essere semplicemente “più terapie”, ma una terapia finalmente più vicina alla biologia reale della malattia.
E forse, proprio per questo, più vicina ai bisogni dei pazienti.
Lo studio
Katharina Schilbach, Christian J Strasburger, What Is the Future of Acromegaly Therapy?, The Journal of Clinical Endocrinology & Metabolism, 2026;, dgag144.
Fratture vertebrali silenziose
Quando si pensa a una frattura, l’immagine che viene in mente è quasi sempre la stessa: una caduta, un trauma, un dolore acuto e improvviso. Ma non tutte le fratture si presentano così. Le fratture vertebrali da fragilità possono svilupparsi in modo molto meno evidente, e proprio per questo passare inosservate.
In alcuni casi non c’è un evento preciso che segna un “prima” e un “dopo”. Può comparire un dolore che sembra un comune mal di schiena, oppure un cambiamento graduale che si attribuisce all’età, alla postura o alla stanchezza.
Ed è per questo che vengono spesso definite silenziose: non perché non abbiano effetti, ma perché possono non essere riconosciute.
Come può succedere
Quando una vertebra è indebolita dalla fragilità ossea, può cedere anche in assenza di un trauma importante. Talvolta basta uno sforzo modesto, un movimento abituale o, in alcuni casi, non c’è neppure un episodio chiaramente identificabile.
Questo sorprende molte persone, perché si tende a pensare che una frattura richieda sempre un evento traumatico evidente. In realtà, nelle ossa fragili, il meccanismo può essere diverso. Ed è proprio questa caratteristica a rendere queste fratture spesso sottodiagnosticate.
Segnali che meritano attenzione
Non sempre il segnale è un dolore intenso. Talvolta è più sottile. Una schiena che sembra cambiare, una postura che si incurva progressivamente, una riduzione dell’altezza, una fatica crescente a restare a lungo in piedi.
Sono cambiamenti che spesso vengono normalizzati. “È l’età”, “sarà artrosi”, “è solo mal di schiena”.
Ma in alcuni casi meritano una valutazione. Non per trasformare ogni dolore in allarme, ma per non perdere segnali che potrebbero avere un significato diverso.
Perché riconoscerle cambia le cose
Una frattura vertebrale non riguarda solo la singola vertebra coinvolta. Può influenzare equilibrio, mobilità, dolore e qualità della vita. Può modificare il modo in cui la colonna distribuisce i carichi e, nel tempo, favorire ulteriori problemi.
Ma c’è un aspetto ancora più importante: una frattura vertebrale può aumentare il rischio di averne altre.
Per questo riconoscerne una non significa solo gestire un evento già avvenuto. Significa spesso intervenire per prevenire ciò che potrebbe succedere dopo.
Perché spesso si scoprono tardi
Il ritardo diagnostico dipende da molti fattori. I sintomi possono essere sfumati. Possono sovrapporsi ad altri disturbi comuni. E talvolta semplicemente non si pensa a questa possibilità.
Questo rende le fratture vertebrali un tema importante anche dal punto di vista della consapevolezza. Perché sapere che esistono è già una forma di prevenzione.
Cosa si può fare
Se c’è un sospetto, il medico può valutare se siano necessari approfondimenti. E se una frattura viene riconosciuta, ci sono diverse possibilità di intervento: dalla gestione del dolore a percorsi riabilitativi, fino alla rivalutazione della protezione dell’osso.
Questo è forse il messaggio più importante: riconoscerle serve perché qualcosa si può fare. E spesso farlo in tempo cambia molto.
Ascoltare i cambiamenti del corpo
Molte persone non notano un singolo evento, ma un cambiamento progressivo. Si sentono meno stabili. Più curve. Più affaticate.
Sono segnali che meritano ascolto. Perché, a volte, il corpo comunica in modo discreto.
E imparare a non ignorarlo è parte della cura.