Con Determina n. 1283/2019 del 27 agosto 2019 “Regime di rimborsabilità e prezzo del medicinale per uso umano Crysvita”, pubblicata in Gazzetta Ufficiale il 5 settembre scorso (GU n.208 del 5-9-2019), l’Agenzia Italiana del Farmaco ha autorizzato l’impiego, in regime di rimborsabilità (classe H) dell’anticorpo monoclonale ricombinante umano burosumab (Crysvita® – titolare A.I.C.: Kyowa Kirin Holdings B.V. – Paesi Bassi).
La specialità medicinale è indicata per il trattamento dell’ipofosfatemia X-linked (XLH) con evidenza radiografica di malattia ossea, nei bambini di età pari o superiore a un anno e negli adolescenti con sistema scheletrico in crescita.
A burosumab è attribuito il requisito dell’innovazione terapeutica condizionata da cui consegue unicamente l’inserimento nei prontuari terapeutici regionali nei termini previsti dalla normativa vigente (art. 10, comma 2, decreto-legge n. 158/2012 convertito in legge n. 189/2012).
Ai fini delle prescrizioni a carico del Ssn, burosumab i centri utilizzatori specificatamente individuati dalle regioni, dovranno compilare la scheda raccolta dati informatizzata di arruolamento che indica i pazienti eleggibili e la scheda di follow-up, applicando le condizioni negoziali secondo le indicazioni pubblicate sul sito dell’agenzia.
Ai fini della fornitura, la classificazione di burosumab è quella di medicinale soggetto a prescrizione medica limitativa, vendibile al pubblico su prescrizione di centri ospedalieri o di specialisti – centri di riferimento autorizzati alla diagnosi e al trattamento dell’ipofosfatemia X-linked (XLH) individuati dalle regioni e province autonome (RRL).
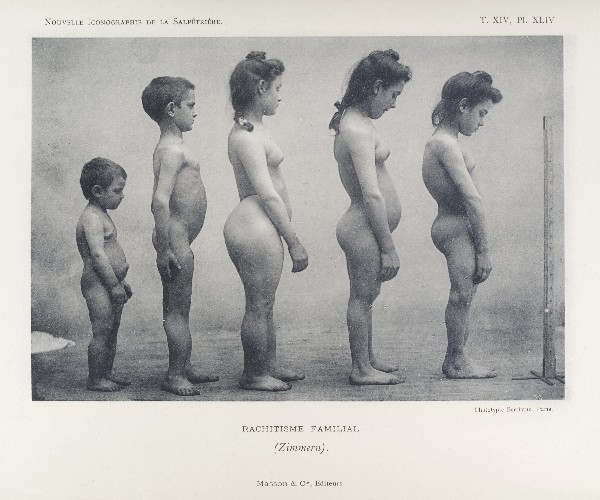
Ipofosfatemia X-linked (XLH)
L’ipofosfatemia legata all’X è la forma più comune di rachitismo genetico ed è caratterizzata da basse concentrazioni circolanti di fosforo che compromettono la mineralizzazione scheletrica e provocano rachitismo nei bambini in crescita e osteomalacia negli adulti.
L’ipofosfatemia legata all’X è causata da mutazioni del PHEX (omologo endopeptidasi regolante il fosfato, legato all’X), che codifica per l’endopeptidasi transmembrana. Sebbene il meccanismo sia incerto, la perdita di PHEX comporta un aumento delle concentrazioni plasmatiche del fattore di crescita dei fibroblasti 23 (FGF23), il membro meglio caratterizzato di una famiglia di ormoni che regolano il fosfato chiamati fosfatonine. L’eccesso di FGF23 determina la maggior parte delle caratteristiche biochimiche e sistemiche dell’ipofosfatemia legata all’X, sebbene altri fattori contribuiscano alla fisiopatologia generale [1].
Burosumab vs terapia convenzionale
La terapia tradizionale per la XLH è basata sull’assunzione di calcitriolo (un metabolita attivo della vitamina D) associato a sali di fosfato inorganico e corregge solo alcune delle alterazioni biochimiche della malattia, senza modificare i meccanismi patogenetici sottostanti, come gli elevati livelli di FGF23, e senza poter intervenire nei processi difettosi di mineralizzazione ossea. Tali terapie richiedono più dosi suddivise nell’arco della giornata e il monitoraggio dei potenziali rischi quali nefrocalcinosi, ipercalciuria e iperparatiroidismo.
Burosumab è un anticorpo monoclonale ricombinante umano progettato per dirigersi specificamente contro il fattore di crescita fibroblastico 23, e nei pazienti con XLH ha dimostrato di poter significativamente ridurre la deformità degli arti inferiori e la gravità generale del rachitismo, oltre a indurre miglioramenti nella funzionalità fisica (ad esempio nella capacità di deambulazione).
Uno studio di fase 3 recentemente pubblicato ha evidenziato miglioramenti clinici significativamente maggiori nella gravità, nella crescita e nei biochimici del rachitismo nei bambini con ipofosfatemia legata all’X trattati con burosumab rispetto a quelli che continuano la terapia convenzionale.
Nello studio Burosumab versus conventional therapy in children with X-linked hypophosphataemia: a randomised, active-controlled, open-label, phase 3 trial [2] sono state confrontate l’efficacia e la sicurezza della terapia convenzionale continua, costituita da fosfato orale e vitamina D attiva, rispetto al passaggio all’anticorpo monoclonale completamente umano contro FGF23 burosumab, nell’ipofosfatemia pediatrica legata all’X.
Nello studio di fase 3 randomizzato, active-controlled, open-label, condotto in 16 siti clinici, sono stati arruolati bambini con ipofosfatemia legata all’X di età compresa tra 1 e 12 anni. I pazienti eleggibili secondo i criteri stabiliti sono stati assegnati in modo casuale (1:1) a ricevere burosumab per via sottocutanea a partire da 0,8 mg/kg ogni 2 settimane (gruppo burosumab) o terapia convenzionale prescritta dai ricercatori (gruppo di terapia convenzionale). Entrambi gli interventi sono durati 64 settimane. L’endpoint primario era la variazione della gravità del rachitismo alla settimana 40, valutata dal punteggio globale Radiographic Global Impression of Change. Tutti i pazienti che hanno ricevuto almeno una dose di trattamento sono stati inclusi nelle analisi primarie e di sicurezza. The trial is registered with ClinicalTrials.gov, number NCT02915705.
Dei 122 pazienti valutati, 61 sono stati arruolati. Di questi, 32 (18 ragazze, 14 ragazzi) sono stati assegnati in modo casuale a continuare a ricevere la terapia convenzionale e 29 (16 ragazze, 13 ragazzi) a ricevere il burosumab. Per l’endpoint primario alla settimana 40, i pazienti nel gruppo burosumab avevano un miglioramento significativamente maggiore nel punteggio globale Radiographic Global Impression of Change rispetto ai pazienti nel gruppo di terapia convenzionale. Eventi avversi considerati potenzialmente, probabilmente o sicuramente correlati al trattamento si sono verificati più frequentemente con burosumab (17 su 29 pazienti – 59%- nel gruppo burosumab contro sette su 32 pazienti – 22% – nel gruppo di terapia convenzionale). Tre eventi avversi gravi si sono verificati in ciascun gruppo, tutti considerati non correlati al trattamento e risolti.
[1] Gordon R, Levine M. Burosumab treatment of children with X-linked hypophosphataemic rickets [pubblicato online 16 maggio 2019]. Lancet. Doi 10.1016/S0140-6736(19)31054-2
[2] Imel E, Glorieux F, Whyte M, et al. Burosumab versus conventional therapy in children with X-linked hypophosphataemia: a randomised, active-controlled, open-label, phase 3 trial [published online May 16, 2019]. Lancet. doi: 10.1016/S0140-6736(19)30654-3