Negli ultimi due decenni, l’introduzione di farmaci biologici antireumatici modificanti la malattia (bDMARD) associati a un approccio treat-to-target ha migliorato notevolmente la gestione dell’artrite reumatoide (RA) [Biologics for rheumatoid arthritis: an overview of Cochrane reviews]; tuttavia, nonostante la significativa riduzione dei danni strutturali articolari, diversi studi hanno dimostrato che gli eventi cardiovascolari (CV) stanno emergendo come la principale causa di morte in questi pazienti, sottolineando così la stretta associazione tra RA e malattia CV (CVD) [Cardiovascular comorbidity in rheumatic diseases].
Per quanto riguarda il ruolo dei tradizionali fattori di rischio CV nella RA, è stata evidenziata un’aumentata associazione tra RA e il metabolismo anomalo del glucosio, ciò che spiega l’elevata prevalenza di diabete di tipo 2 (T2D) e di insulino-resistenza (IR) in questi pazienti [Prevalence of type 2 diabetes and impaired fasting glucose in patients affected by rheumatoid arthritis].
L’interleuchina-1β (IL-1β), IL-6 e il fattore di necrosi tumorale (TNF), che sono coinvolti nella patogenesi della RA, possono anche svolgere un ruolo fondamentale nello sviluppo dell’IR [Targeting inflammation in the treatment of type 2 diabetes: time to start].
È interessante notare che l’aumento dei livelli di glucosio stressa le isole pancreatiche e i tessuti sensibili all’insulina, portando all’iperproduzione di IL-β. Questo IL-1β sovraespresso contribuisce alla patogenesi del T2D, causando disfunzione e apoptosi delle cellule β, con conseguente riduzione della produzione di insulina. Inoltre, IL-1β potrebbe inibire direttamente la secrezione di insulina stimolata dal glucosio e innescare la via intrinseca apoptotica mitocondriale nelle cellule β.
La recente conoscenza del contributo dei processi infiammatori alla patogenesi del T2D ha suggerito nuove strategie terapeutiche antidiabetiche in cui i bDMARD, che sono comunemente usati nel trattamento della RA, possono essere efficaci nel migliorare le anomalie del glucosio. Tuttavia, nonostante il crescente numero di prove provenienti da studi preclinici e clinici che confermano il ruolo del targeting per citochine infiammatorie nel miglioramento degli esiti clinici e di laboratorio nei pazienti T2D, nessuno studio clinico specificamente progettato per valutare l’esito glicemico in pazienti con RA e T2D è stato finora pianificato [Anti-interleukin-1 treatment in patients with rheumatoid arthritis and type 2 diabetes (TRACK): A multicentre, open-label, randomised controlled trial].
Basandosi sull’approccio treat-to-target che accomuna RA e T2D, l’individuazione di un singolo trattamento che controlla entrambe queste malattie sembra essere una scelta promettente per migliorare la gestione dei pazienti con RA e T2D [IL-1β at the crossroad between rheumatoid arthritis and type 2 diabetes: may we kill two birds with one stone?]. L’aderenza alla terapia è infatti inversamente proporzione al numero di farmaci assunti dai pazienti in politerapia e ogni singola strategia terapeutica che tratta contemporaneamente due malattie diverse può anche aiutare i decisori delle politiche sanitarie a ottimizzare i costi mantenendo la qualità dei trattamenti.
A partire da queste considerazioni, per verificare se l’inibizione dell’IL-1 con anakinra potesse indurre il miglioramento dei parametri glicemici e infiammatori nei partecipanti con RA e T2D, rispetto ai partecipanti trattati con un inibitore del TNF (TNFi), ricercatori coordinati dalla Cattedra di Reumatologia del Dipartimento di Biotecnologie e Scienze Cliniche Applicate dell’Università de L’Aquila hanno condotto uno studio multicentrico, randomizzato, in aperto, prospettico, controllato, a gruppi paralleli. Lo studio è stato pubblicato sulla rivista PLOS Medicine Anti-interleukin-1 treatment in patients with rheumatoid arthritis and type 2 diabetes (TRACK). A multicentre, open-label, randomised controlled trial.
Metodi e risultati
Lo studio multicentrico, open-label, randomizzato ha coinvolto e seguito per sei mesi (tra il 2013 e il 2016) 41 pazienti con RA e T2D in 12 unità reumatologiche italiane. I partecipanti sono stati trattati con anakinra o con un TNFi (come ad es. adalimumab, certolizumab pegol, etanercept, infliximab o golimumab) e l’end point primario era la variazione della percentuale di emoglobina glicata (HbA1c%) (EudraCT: 2012-005370-62 ClinicalTrial.gov: NCT02236481).
In totale, sono stati randomizzati 41 partecipanti con RA e T2D e ne sono stati trattati 39 ammissibili (età 62,72 ± 9,97 anni; 74,4% sesso femminile). La maggior parte dei partecipanti era affetta da artrite reumatoide sieropositiva (fattore reumatoide e/o anticorpi anti peptide ciclico citrullinato [ACPA] 70,2%) con malattia attiva (Disease Activity Score-28 [DAS28]: 5,54 ± 1,03; proteina C reattiva 11,84 ± 9,67 mg/L, rispettivamente). Tutti i partecipanti avevano T2D (HbA1c%: 7,77 ± 0,70; glicemia a digiuno: 139,13 ± 42,17 mg).
Dopo i primi sei mesi di follow-up, l’importante differenza nel raggiungimento dell’end point principale – confermato da un’analisi ad hoc non pianificata che ha mostrato la superiorità di anakinra rispetto agli altri TNFis – ha portato a fermare lo studio per beneficio anticipato.
I partecipanti al gruppo anakinra hanno avuto una riduzione significativa dell’HbA1c%, in un modello misto lineare non aggiustato, dopo tre mesi (β:−0,85; p<0,001; IC al 95% da −1,28 a −0,42) e dopo sei mesi (β:−1,05; p<0,001; IC al 95% da −1,50 a −0,59). Risultati simili sono stati osservati modificando il modello per rilevanti confonditori clinici di RA e T2D (sesso maschile, età, positività ACPA, uso di corticosteroidi, durata della RA, durata T2D, uso di un farmaco antidiabetico orale, indice di massa corporea [BMI]) dopo tre mesi (β:−1,04; p<0,001; IC al 95% da −1,52 a −0,55) e dopo sei mesi (β:−1,24; p<0,001; IC al 95% da −1,75 a −0,72). I partecipanti al gruppo TNFi hanno avuto una leggera riduzione non significativa dell’HbA1c%. Supponendo che la soglia di successo sia HbA1c% ≤ 7, è stata considerata una riduzione del rischio assoluto (ARR) = 0,42 (tasso di eventi sperimentali = 0,54; tasso di eventi di controllo = 0,12); pertanto, è stato stimato, arrotondando per eccesso, un numero necessario per il trattamento (NNT) = 3.
Per quanto riguarda la RA, è stata osservata una riduzione progressiva dell’attività della malattia in entrambi i gruppi.
Non sono stati osservati eventi avversi gravi, episodi ipoglicemici o decessi. Reazioni locali nel sito di iniezione hanno portato alla sospensione di 4 (18%) partecipanti trattati con anakinra. Inoltre, sono state osservate infezioni non gravi, tra cui influenza, rinofaringite, infezione del tratto respiratorio superiore, infezione del tratto urinario e diarrea in entrambi i gruppi.
Interruzione per beneficio precoce
Inaspettatamente, l’ipotesi di studio è stata dimostrata prima della fine dello studio, con una maggior percentuale di partecipanti trattati con anakinra che hanno soddisfatto l’end point primario (variazione dei livelli di HbA1c% tra la baseline e le visite successive, con differenza assoluta tra i due bracci valutata significativa, in accordo con la letteratura, se pari allo 0,25%) rispetto ai partecipanti trattati con TNFi.
I risultati suggeriscono che l’inibizione dell’IL-1 da parte di anakinra può consentire il targeting terapeutico di entrambi i disturbi e l’uso di un singolo agente può aiutare nella gestione delle malattie infiammatorie e metaboliche.
Nei partecipanti trattati con anakinra è stata osservata una significativa riduzione di HbA1c%, che suggerisce l’efficacia metabolica dell’inibizione dell’IL-1. I risultati sono in linea con quelli di un precedente studio [Interleukin-1–Receptor Antagonist in Type 2 Diabetes Mellitus] in quanto i partecipanti al T2D trattati con anakinra hanno mostrato una diminuzione di HbA1c e del rapporto tra proinsulina e insulina. È interessante notare che l’estensione di questo studio ha dimostrato che questo miglioramento dei parametri glicemici era ancora presente 39 settimane dopo l’interruzione di anakinra, confermando che anakinra è in grado di migliorare la secrezione di insulina. Inoltre, confrontando i risultati dello studio in oggetto con il precedente studio su T2D [Interleukin-1–Receptor Antagonist in Type 2 Diabetes Mellitus], è stata osservata una riduzione più evidente dell’HbA1c%, suggerendo che i meccanismi patogeni infiammatori di T2D potrebbero essere esagerati nel contesto della RA. In effetti, è stata osservata una correlazione significativa tra i livelli decrescenti di HbA1c% e la riduzione dell’attività della malattia. Al contrario, la terapia con anakinra non ha mostrato alcun effetto nei partecipanti con diabete di tipo 1 (T1D), probabilmente perché l’insulite pancreatica nel T1D è principalmente guidata da un processo autoimmune-mediato, piuttosto che da un processo autoinfiammatorio, come suggerito in T2D, quindi non supporta i benefici dell’inibizione dell’IL-1 nel T1D. Infatti, durante il T2D, i livelli eccessivi di nutrienti, tra cui glucosio e acidi grassi liberi, stressano le isole pancreatiche e i tessuti sensibili all’insulina, portando all’iperproduzione di IL-β tramite l’attivazione inflammasoma NLRP3, un sensore di pericolo metabolico. Inoltre, alte concentrazioni di glucosio inducono la sovraespressione del recettore FAS proapoptotico sulle cellule β. Di conseguenza, IL-1β e FAS possono contribuire, da un lato, alla compromissione indotta dal glucosio della funzione secretoria delle cellule β e, dall’altro, può portare all’apoptosi delle cellule β.
In questo studio, nei partecipanti trattati con anakinra, parallelamente alla riduzione dell’HbA1c%, è stata osservata una riduzione di FPG (fasting plasma glucose). Nonostante il miglioramento dell’HbA1c% e dell’FPG nei partecipanti trattati con anakinra, non è stata osservata ipoglicemia sintomatica. In effetti, le limitazioni dei trattamenti antidiabetici, come l’insulina e le sulfoniluree, possono includere l’insorgenza di ipoglicemia sintomatica imprevedibile. Al contrario, è stato suggerito che, a seguito del miglioramento della funzione delle cellule β, usando l’antagonismo dell’IL-1, queste cellule dovrebbero rilasciare quantità adeguate di insulina dopo la stimolazione metabolica, riducendo così il rischio di ipoglicemia. Infine, il BMI (body mass index) dei partecipanti è rimasto stabile, escludendo così la possibilità che il miglioramento dei parametri metabolici possa essere associato a un effetto anoressigenico di anakinra.
Per quanto riguarda il trattamento con TNFi, durante il follow-up non è stato osservato un effetto statisticamente significativo sull’HbA1c%. Nonostante l’evidenza sperimentale suggerisca un possibile ruolo del TNF nella regolazione della produzione e della funzione dell’insulina, la traduzione dagli studi di base al contesto clinico non è riuscita a confermare un ruolo del TNFi nel trattamento del T2D umano.
In base a questi risultati, è stato deciso, con l’ulteriore supporto di diverse evidenze statistiche, di interrompere anticipatamente lo studio per motivi relativi all’efficacia.
Lo studio suggerisce che, nei pazienti con RA e T2D, anakinra potrebbe essere considerato un trattamento mirato, portando a un miglioramento dei parametri metabolici e dei segni infiammatori, adattando il trattamento medico alle caratteristiche individuali. Inoltre, considerando l’effetto confermato dell’inibizione dell’IL-1 nella prevenzione delle malattie cardiovascolari, è possibile suggerire che l’inibizione dell’IL-1 possa ridurre l’incidenza del rischio cardiovascolare nella RA. I risultati del studio potrebbero anche aprire la strada a successivi studi di conferma che analizzano l’efficacia della strategia terapeutica mirata all’IL-1 nella RA con T2D.
Limitazioni dello studio
Lo studio presenta alcune limitazioni, dovute principalmente al design in aperto e a un’analisi ad interim non precedentemente pianificata, che è più soggetta a distorsioni rispetto a uno studio controllato in doppio cieco.
Inoltre, secondo il disegno dello studio e la legge italiana, erano consentiti solo test di routine consolidati per la gestione di T2D e/o CVD e non è stato quindi possibile pianificare alcune valutazioni, come il peptide C, il plasma endogeno insulina IL-1Ra, così come marcatori di laboratorio della disfunzione endoteliale, che sarebbero di interesse.
A causa del progetto di studio della “vita reale”, il risultato potrebbe essere stato influenzato dalla continuazione dell’utilizzo di altri farmaci, d’altra parte la randomizzazione al placebo dei partecipanti affetti da una malattia attiva, limitando il possibile beneficio di terapie standard ben note, avrebbe potuto sollevare alcuni problemi etici.
Dimostrando che l’end point primario è stato raggiunto solo nel gruppo anakinra, i risultati hanno mantenuto la loro rilevanza statistica nonostante il basso numero di pazienti arruolati, risolvendo parzialmente risolto il problema scientifico.
Conclusioni
Lo studio ha permesso di osservare un beneficio dell’inibizione dell’IL-1 nei partecipanti con AR e T2D, raggiungendo gli obiettivi terapeutici di entrambe le malattie.
I partecipanti trattati con anakinra hanno raggiunto l’end point primario (riduzione dell’HbA1c%) in pochissimo tempo. Nei partecipanti trattati con TNFi non è stata osservata una riduzione significativa dell’HbA1c% .
I risultati suggeriscono che l’inibizione dell’IL-1 può essere considerata un trattamento mirato per i pazienti con RA e T2D.
La gestione della malattia infiammatoria e della comorbilità metabolica da parte di un agente che inibisce l’IL-1 può comportare un conseguente impatto benefico sulla compliance dei partecipanti, sul loro rischio cardiovascolare generale (CV) e sull’onere dei costi sanitari.
Tuttavia, sono necessari altri studi – che potrebbero includere l’uso di anakinra in monoterapia – per valutare ulteriormente l’uso di inibitori dell’IL-1 in pazienti con AR e T2D e per valutare i risultati a lungo termine sulla malattia cardiovascolare.
Ruscitti P, Masedu F, Alvaro S, Airò P, Battafarano N, Cantarini L, et al. (2019) Anti-interleukin-1 treatment in patients with rheumatoid arthritis and type 2 diabetes (TRACK): A multicentre, open-label, randomised controlled trial. PLoS Med 16(9): e1002901.




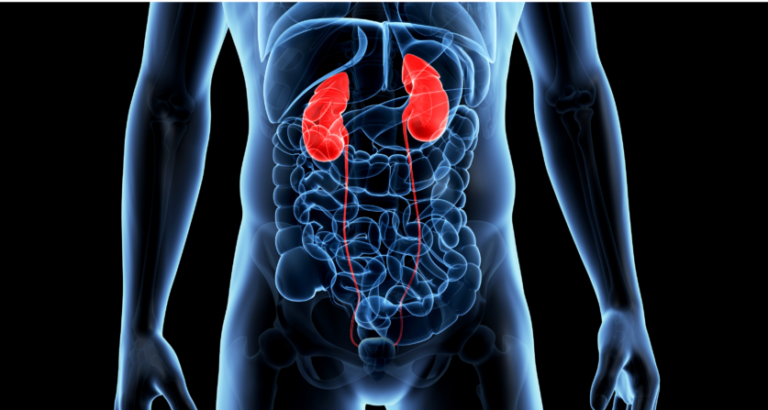




![Femmina di 14 anni con XLH (PHEX: c. [151C> T]; [=] p. [Gln51 *]) diagnosticata a 7 mesi di età. (A) Radiografia della mano sinistra e del polso alla diagnosi con alterazioni rachitiche del raggio distale e dell'ulna e dell'aspetto livido dell'osso. (B) Radiografia del ginocchio destro a 18 mesi mentre trattata con fosfato e calcitriolo. Vi sono sfilacciamenti e distorsioni alle metafisi e una coppettazione precoce notata al femore distale, nonché alla tibia e al perone prossimale. (C) A 14 anni, è stata gestita con fosfato e calcitriolo. Aveva bassa statura, ALP normale e lieve aumento della PTH. I sintomi includevano dolore alla caviglia persistente e andatura ondeggiante. C'era anche un inchino laterale sia del femore che della tibia con l'allargamento della placca prossimale di crescita tibiale. (D) Radiografia della mano sinistra all'età di 14 anni che mostra un allargamento del raggio prossimale e delle placche di crescita dell'ulna con evidenza di alterazioni rachitiche.](https://bonehealth.it/storage/2019/11/ipofosfatemia.png)