Un recente revisione della letteratura riassume le ultime scoperte sul ruolo che i mastociti hanno nel quadro generale del metabolismo osseo.
Mastociti, attori fondamentali del sistema immunitario…
I mastociti (MC) sono cellule immunitarie tessuto-specifiche e sono note per il loro ruolo nell’induzione delle risposte allergiche. Sono facilmente individuabili dalla presenza di un gran numero di granuli nel citoplasma, quali istamina, eparina, varie citochine (ad es. il tumor necrosis factor, TNF) e chemochine, interleuchina 6 (IL-6), enzimi (ad es. chimasi e triptasi) ed alcuni fattori di crescita (come il fattore di crescita endoteliale dei vasi, VEGF, o il fattore di crescita dei fibroblasti, FGF).
Essi sono fondamentali nella risposta immunitaria in quanto possiedono la capacità di alterare la produzione di muco da parte del tessuto epiteliale (bloccando il patogeno) e, modificando la permeabilità vascolare, richiamano altri tipi di cellule immunitarie nella sede dell’infezione.
Infine, sembrano avere anche un ruolo importante nel processo di rimarginazione delle ferite, grazie alla presenza nei loro granuli di molti fattori angiogenici (VEGF, FGF, TNF-α, eparina, istamina e interleuchina 8).
… e nel turnover osseo
Si è sempre sospettato che i mastociti ricoprano un ruolo importante anche nell’omeostasi del tessuto osseo, in quanto un numero importante di queste cellule è presente sulla superficie endocorticale delle ossa e molti dei granuli presenti nel loro citoplasma (ad es. eparina, istamina e varie proteasi) possono avere un ruolo anche nella fisiologia del tessuto osseo.
Molti dei mediatori dei mastociti sono in grado di indurre o modulare diversi effetti ostemetabolici, promuovendo e/o inibendo l’attività degli osteblasti (ad es. il fattore di crescita trasformante β, TGFβ) e l’osteoclastogenesi (tramite l’istamina, il TNF e l’IL-6).
Poiché non sono note molte condizioni che riducono o portano alla totale assenza di mastociti, la maggior parte dei dati a nostra disposizione riguardo il loro ruolo fisiologico nel turnover osseo deriva da studi in vitro oppure da modelli murini. Tra questi ricordiamo:
- KitW/W-v e KitW-sh/W-sh: Modelli murini con mutazioni per c-Kit, nei quali il rimodellamento osseo era decisamente ridotto per via del basso numero di osteoclasti e l’alta presenza di osteoblasti.
- KitlSl/Sl-d: Modelli murini dove è mutato il ligando SCF e che presentano un turnover osseo molto marcato per via dell’alta attività degli osteoclasti rispetto a quella degli osteoblasti.
Ad ogni modo, è bene far notare che c-Kit è espresso anche in altri tipi cellulari (ad esempio nelle cellule ematopoietiche) oltre che essere molto importante anche per lo sviluppo degli osteoclasti. Risulta quindi difficile distinguere un effetto sull’omeostasi ossea dovuta esclusivamente all’azione dei mastociti.
È inoltre importate sapere che uno studio condotto proprio dal gruppo di Ragipoglu ha evidenziato come modelli murini Mcpt-5 Cre R-DTA, deficitari del corrispettivo murino dei mastociti, non presentavano differenze significative nella struttura ossea macroscopica e microscopica né avevano differenti numeri di osteoclasti o osteoblasti se comparati con quelli di topi wildtype, suggerendo una possibile ridondanza di questo sistema di regolazione.
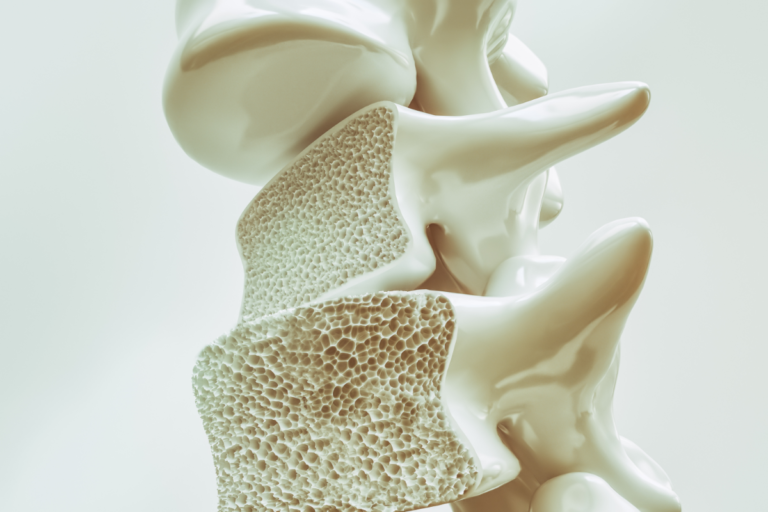
Appare quindi evidente come i dati sul ruolo dei mastociti nella regolazione del turnover osseo siano in certi casi contraddittori e che la mancanza di condizioni patologiche umane che abbassino la conta dei mastociti renda ancora più difficile comprendere il reale funzionamento di questo sistema. Tuttavia, pazienti con patologie che aumentano la conta delle MC spesso presentano anche disturbi dell’omeostasi ossea (come per esempio l’osteoporosi), suggerendo una funzione importante di queste cellule del sistema immunitario.