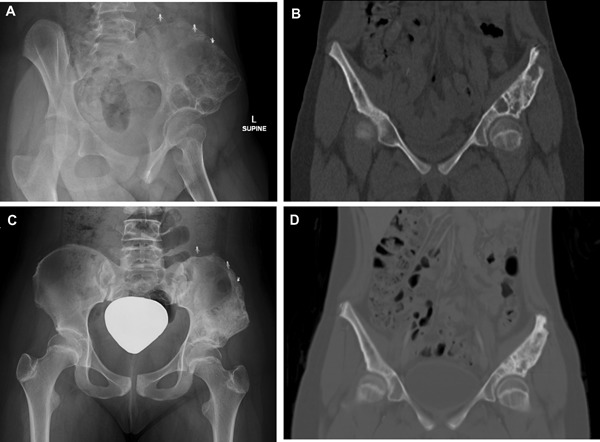
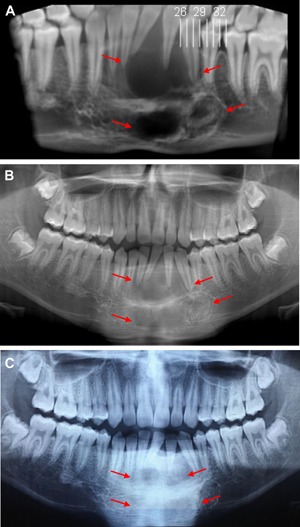
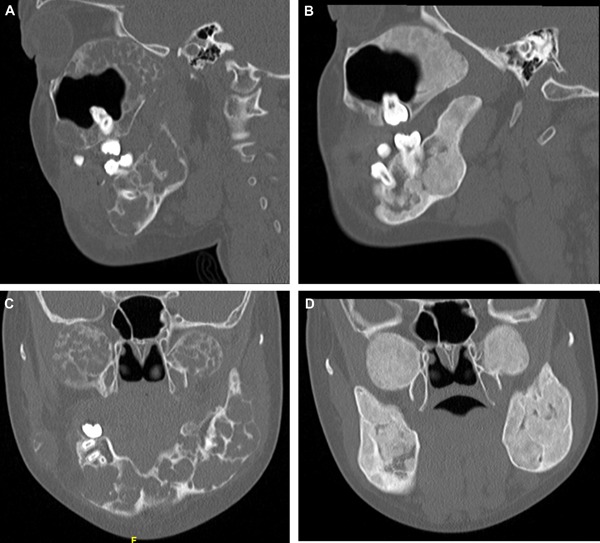
Le patologie del parodonto sono tra le più comuni malattie che affliggono la popolazione. Causano una reazione infiammatoria che coinvolge svariati tessuti che circondano i denti, quali gengiva, legamenti parodontali e osso alveolare e possono estendersi a livello sistemico.
La parodontite insorge a causa dell’accumulo di biofilm di placca a livello dentale, ove la dismicrobiosi provoca una risposta distruttiva infiammatoria locale e quindi la degenerazione dei tessuti. Questa risposta dell’ospite alle variazioni batteriche presenti nel biofilm causa un’infiammazione che si cronicizza nel tempo. Diversi studi hanno dimostrato che lo stato infiammatorio non risulta limitato localmente al parodonto, ma provoca, a causa del rilascio di citochine pro-infiammatorie e mediatori dell’infiammazione, una risposta sistemica. Anche la parodontite, così come altre malattie infiammatorie croniche, svolge un ruolo sistemico e può quindi essere associata allo sviluppo di alcune condizioni, tra cui disordini metabolici e patologie cardiovascolari. Tra queste da considerare con particolare attenzione il diabete mellito di tipo 2.
La reazione infiammatoria cronica causata dalla parodontite risulta un fattore di rischio per lo sviluppo di diabete e delle sue complicanze, poiché aumenta l’insulino-resistenza e la disfunzione endoteliale.
Parodontite e diabete, relazione bidirezionale
È stato suggerito che la parodontite e il diabete sono due patologie strettamente associate tra loro e che hanno una relazione bidirezionale.
Il rischio di parodontite in persone affette da diabete è incrementato di 2-3 volte rispetto agli individui sani e risulta inversamente proporzionale al controllo glicemico. Inoltre, diversi studi hanno dimostrato che gli individui con uno scarso controllo glicemico (HbA1c >9,0%) sviluppano frequentemente una patologia del parodonto più severa degli individui con normale metabolismo glucidico.
La relazione diabete-parodontite risulta bidirezionale: l’infiammazione cronica e sistemica derivata dalla patologia parodontale o dalla scarsa igiene orale possono avere un ruolo nell’insorgenza del diabete mellito di tipo 2 attraverso diversi meccanismi: il dismicrobismo e la produzione di citochine e mediatori dell’infiammazione (es. TNF-α e CPR). Questi, dopo esser stati prodotti localmente, entrano in circolo contribuendo a creare un quadro di infiammazione sistemica con conseguente insulino-resistenza, incremento della glicemia, dei valori di emoglobina glicata (HbA1c) e incremento del rischio di sviluppare diabete o peggiorare il compenso glicometabolico.
Effetti della parodontite sul controllo glicemico e su rischio di diabete mellito di tipo 2
In individui non affetti da diabete:
– La parodontite si associa a livelli più elevati di emoglobina glicata, alterata glicemia a digiuno e alterata tolleranza al glucosio rispetto a individui che non presentano patologie parodontali
– La presenza di parodontite severa è associata a un rischio statisticamente significativo più elevato di sviluppare il diabete (Hazard Ratio 1.19-1.33, corrispondente a un incremento del rischio del 19-33%) rispetto alla popolazione sana
dati estrapolati da “Graziani et al.; J Clin Paronontal 2018”
Parodontite e rischio di complicanze diabetiche
La parodontite è inoltre associata a un aumentato rischio di complicanze diabetiche.
L’82% dei pazienti diabetici con parodontopatia severa sperimenta un evento cardiovascolare o cerebrovascolare maggiore oppure una vasculopatia periferica, rispetto al 21% dei pazienti diabetici senza patologia infiammatoria parodontale.
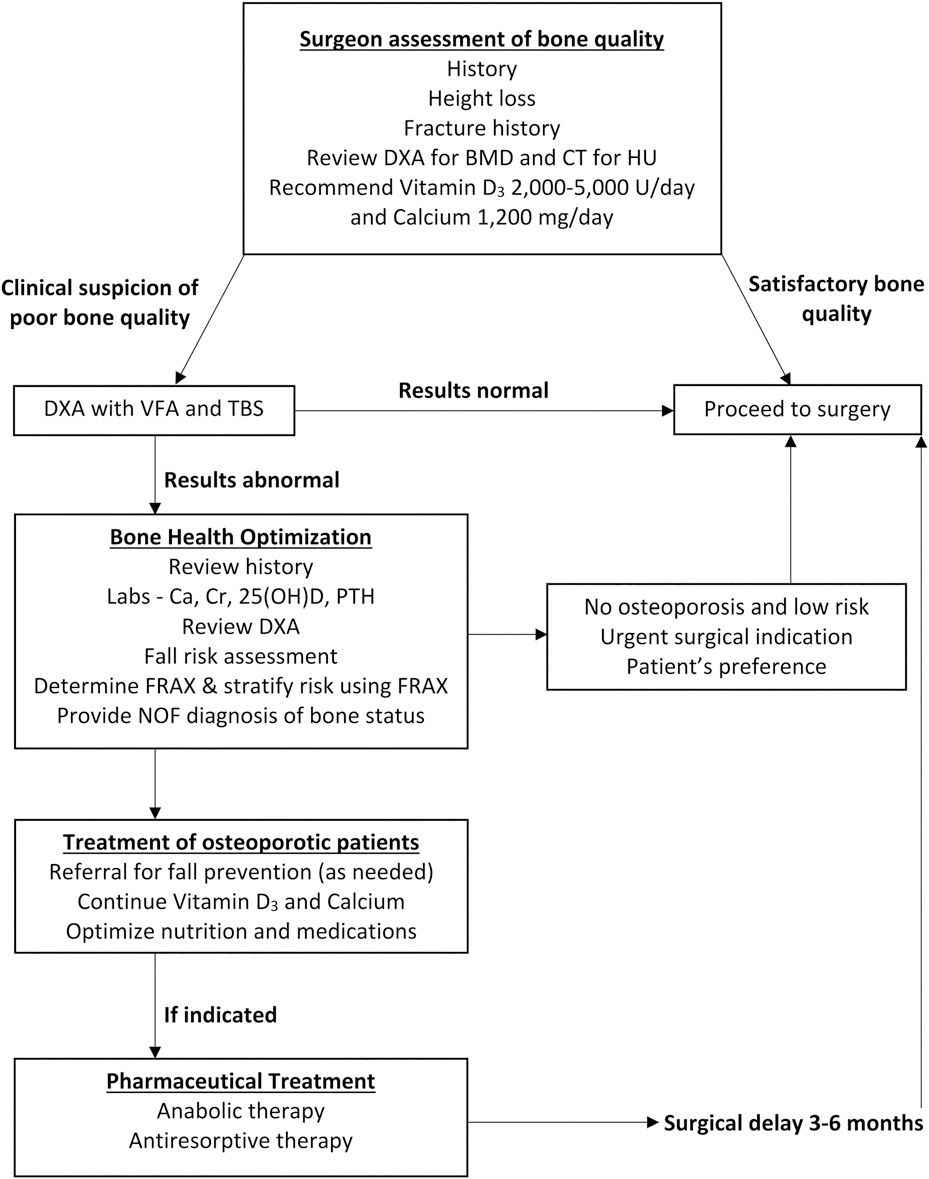
Diversi studi hanno valutato l’impatto del trattamento della patologia infiammatoria parodontale. Due revisioni della Cochrane del 2010 e 2015 hanno mostrato riduzione dei livelli di HbA1c già a tre mesi dal trattamento efficace della parodontopatia. Lo stesso dato è stato confermato da una recente metanalisi che ha evidenziato una riduzione significativa, di 3-7 mmol/mol, nei primi tre mesi dopo il trattamento, ulteriormente confermata, seppur in minor misura, a sei mesi dal trattamento. La riduzione dei batteri sottogengivali porta a una riduzione dei batteri circolanti sistemici e dei loro prodotti con conseguente riduzione di citochine pro-infiammatorie e mediatori (Figura 1).
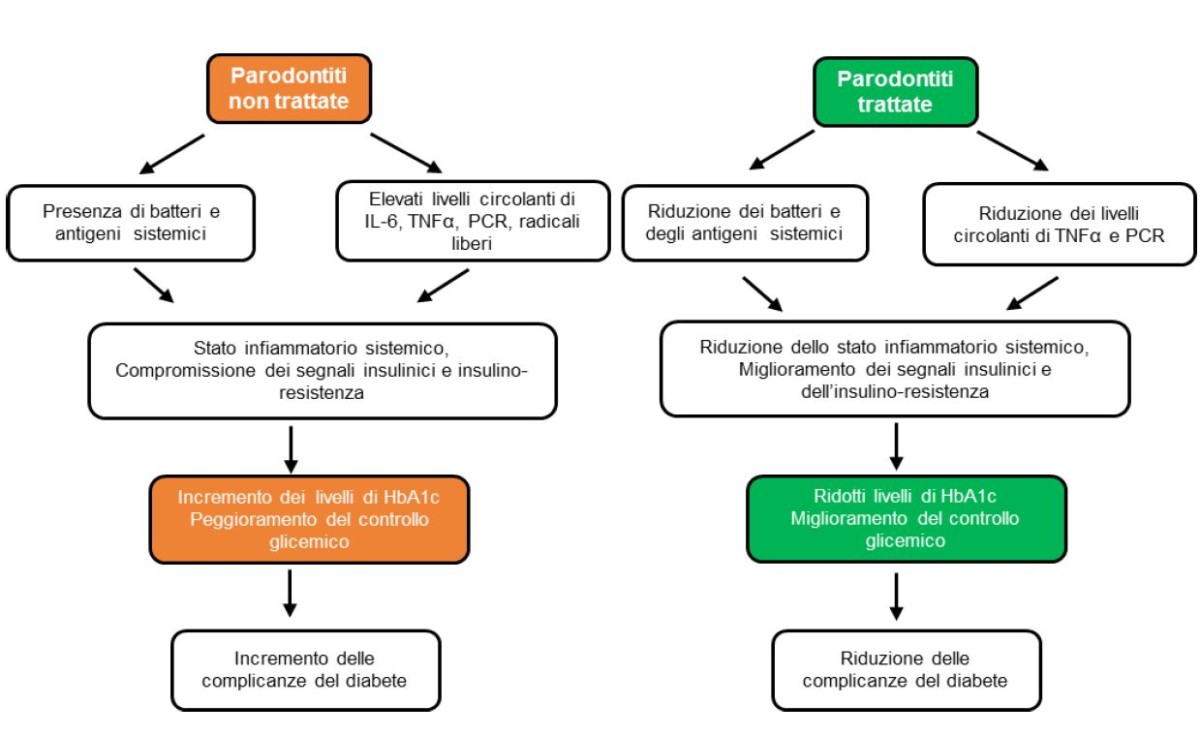
della patologia parodontale sul controllo glicometabolico.
A: Nelle parodontiti non trattate, i batteri, gli antigeni batterici, i mediatori dell’infiammazione e le citochine infiammatorie entrano in circolo e contribuiscono al mantenimento di uno stato infiammatorio sistemico. Questo causa una compromissione dei segnali insulinici che porta a insulino-resistenza, aumento dei livelli di HbA1c e di complicanze del diabete.
B: Dopo trattamento e riduzione dell’infiammazione locale, i livelli di batteri circolanti, antigeni, citochine e mediatori dell’infiammazione si riducono. Di conseguenza lo stato infiammatorio sistemico si riduce e migliorano i parametri glicometabolici di insulino-resistenza e HbA1c, così come si riducono le complicanze associate al diabete. CRP, proteina reattica-C; HbA1c, emoglobina glicata; IL-6, interleuchina-6; TNF-α, fattore di necrosi tumorale-α.
Polak D et al; J Clin Periodontol 2018
Raccomandazioni cliniche
Questi dati permettono di trarre delle raccomandazioni cliniche da inserire nella routine:
- Gli operatori sanitari medici e gli odontoiatri dovrebbero essere consapevoli della relazione bidirezionale tra parodontite e diabete e dovrebbero comunicare queste informazioni ai pazienti
- I professionisti medici dovrebbero chiedere ai pazienti diabetici notizie in merito alla loro salute orale e sui sintomi della parodontite, raccomandare una valutazione odontoiatrica e iniziare una collaborazione con i colleghi
- I professionisti dentali devono eseguire un monitoraggio periodontale periodico nei pazienti con diabete, chiedere informazioni sul controllo glicemico (ad es. livelli di HbA1c) e collaborare con il team medico
- I professionisti dentali potrebbero prendere in considerazione la valutazione del rischio di diabete quando sospettato e collaborare con il medico in caso di evidenza di aumento del rischio di diabete.
Letture consigliate
- Kinane DF, Stathopoulou PG, Papapanou PN (2017) Periodontal diseases. Nat Rev Dis Primers 3:17038
- Yoonkyung Chang, Ji Sung Lee, Ki-Jung Lee, Ho Geol Woo, Tae-Jin Song (2020) Improved oral hygiene is associated with decreased risk of new-onset diabetes: a nationwide population-based cohort study . Diabetologia https://doi.org/10.1007/s00125-020-05112-9
- Linden GJ et al; Periodontal systemic associations: review of the evidence; Periodontol 2013
- Mealey BL et al; Diabetes mellitus and periodontal disease; Periodontol 2000- 2007
- Aguilar-Salinas et al; Recent advances in managing/understanding the metabolic syndrome; F1000 Research 2019
- Polak D et al; An update on the evidence for pathogenic mechanisms that may link periodontitis and diabetes. J Clin Periodontol 2018
- Makkar H et al; periodontal, metabolic, and cardiovascular disease: Exploring the role of inflammation and mental health; Pteridines 2018
- Simpson TC et al; Treatment of periodontal disease for glycaemic control in people with diabetes; Cochrane Database of Systematic Reviews 2010
- Sinmpson TC et al; Treatment of periodontal disease for glycaemic control in people with diabetes mellitus; Cochrane Database of 2015
- Madianos et al; An update of the evidence on the potential impact of periodontal therapy on diabetes outcomes; J Clin Periodontol 2018