Per osteoporosi secondaria si intende una osteoporosi determinata da una patologia sottostante o da farmaci che influenzano negativamente la massa e/o la qualità ossea, causando un aumento del rischio fratturativo.
Fattori secondari e malattie sottostanti nell’osteoporosi ad esordio precoce
Tra i fattori che possono fare insorgere un’osteoporosi di tipo secondario nel giovane adulto troviamo:
- COPD (broncopneumopatia cronica ostruttiva)
- DMD (distrofia muscolare di Duchenne)
- HAART (terapia antiretrovirale altamente attiva)
- HIV (virus dell’immunodeficienza)
- IBD (sindrome dell’intestino infiammato)
- OST (terapia a soppressione ovarica)
Le sopracitate malattie o terapie non sono le uniche coinvolte, ma le più frequenti. Quando si ha il sospetto di una osteoporosi secondaria, una volta effettuata una accurata anamnesi del paziente e della storia patologica della sua famiglia, si procede alle analisi di laboratorio di I livello, in accordo con le principali linee guida intersocietarie italiane. Nel 90% dei casi questi esami escludono forme di osteoporosi secondaria, ma qualora rimanesse il dubbio sono giustificate analisi più approfondite.
Esami di I livello
Per quanto riguarda gli esami di primo livello, l’analisi del Calcio è sicuramente la prima da fare, per valutare una eventuale ipercalemia. Se i livelli di calcio nel siero sono inappropriatamente alti viene fatta un’ulteriore misurazione della creatinina sierica che, qualora si rivelasse alta, sarebbe un chiaro sintomo di iperparatiroidismo primario. L’iperparatiroidismo consiste in un eccesso del paratormone nel sangue dovuto a un’iperattività delle ghiandole paratiroidi, e un eccesso di calcio nel siero porta a un malassorbimento della vitamina D oltre che a una alterazione del ciclo osseo, favorendo l’attività degli osteoclasti.
La seconda analisi più frequente che viene svolta è quella del Fosforo. L’85% dei fosfati totale si concentra nelle ossa, sottoforma di idrossi-apatite, mentre il 15% è extra-scheletrico, sottoforma di ATP, fosfolipidi e acidi nucleici. La fosfatemia (valori normali 2.5-4.5 mg/dL) è controllata in parte dalla calcemia ma è soprattutto influenzata dal contenuto di fosforo nella dieta.
Il fibroblast growth factor 23 (FGF-23) fa parte della classe delle fosfatonine, una nuova classe di ormoni in grado di regolare riassorbimento tubulare ed escrezione urinaria dei fosfati. È una glicoproteina di derivazione ossea (osteociti), la cui sintesi è modulata da PTH, calcitriolo e fosfato. FGF23 si lega a un “signaling complex”, composto dal co-recettore α-Klotho (KL) e dal recettore per il FGF-23 (FGF-R). KL è espresso solo in alcuni tessuti, quali il plesso corioideo, le paratiroidi e il rene; il complesso KL-FGFR sembra essere coinvolto nella modulazione del FGF-23, che promuove l’escrezione renale di fosforo e ne riduce l’assorbimento intestinale, portando quindi a un’ipofosfatemia, a sua volta concausa dell’insorgenza di osteoporosi secondaria. L’ipofosfatemia può essere indotta anche da neoplasie: sono stati descritti casi di neoplasie maligne con metastasi e recidive associate a un incremento di FGF-23, causando una ipofosfatemia biochimicamente indistinguibile da quella indotta da altre cause FGF-23 dipendenti. La terapia dell’ipofosfatemia da perdita renale mediata da FGF-23 richiede sia il fosforo sia il calcitriolo, in quanto l’FGF-23 determina da un lato perdita renale di fosforo e dall’altro inibizione della sintesi renale di calcitriolo.
Esami di II livello
Per cercare i fattori secondari coinvolti nell’osteoporosi secondaria tra gli esami di laboratorio suggeriti ci sono quelli per il diabete mellito. Questa malattia è nota per essere una causa scatenante dell’osteoporosi secondaria, ma è anche collegata più in generale alla fragilità ossea. Sono stati svolti infatti diversi studi sull’associazione tra diabete mellito e rischio di frattura, ed è stata dimostrata (sia negli uomini che nelle donne) una forte incidenza di frattura del bacino in pazienti affetti da diabete di tipo 1 rispetto al diabete di tipo 2. I pazienti con diabete che non sviluppano una osteoporosi secondaria, hanno comunque spesso dei disturbi a livello della conformazione ossea, in particolare la microarchitettura trabecolare è conservata ma aumenta la porosità corticale.
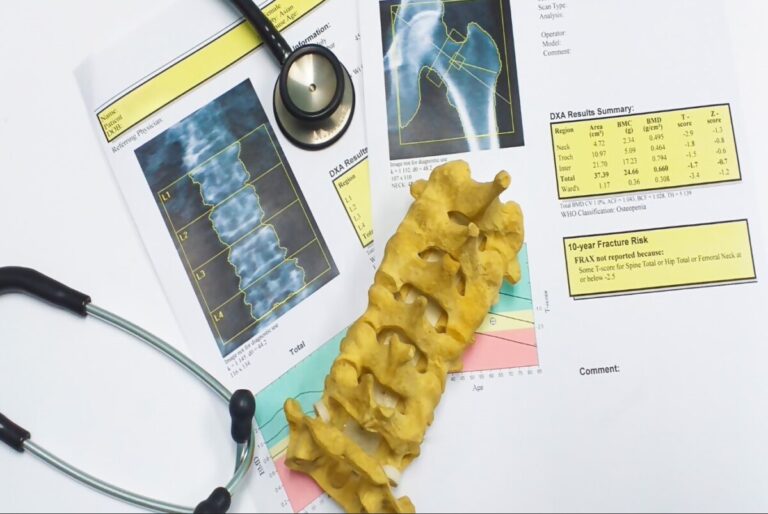
È importante ricordare che la presenza di fattori di rischio tradizionali per fratture osteoporotiche, insieme a quella di fattori di rischio specifici del diabete, dovrebbe essere indagata durante ogni visita diabetologica, indipendentemente dal tipo di diabete. I pazienti affetti da diabete mellito di tipo 1 presentano un alto rischio di frattura già in giovane età, per questo motivo viene riportato come causa di osteoporosi secondaria giovanile, e la diagnosi viene effettuata tramite DXA che, essendo una metodica a bassa emissione di raggi X, può essere eseguita anche in età pediatrica.
Inoltre la terapia insulinica esercita un’azione centrale nel metabolismo osseo, confermato dalla presenza di un recettore insulinico sulla membrana di osteoblasti ed osteoclasti; studi in vitro e in vivo dimostrano un effetto anabolico sull’osso, mentre evidenze cliniche (nel diabete mellito di tipo 2) non confermano un effetto sulla BMD ma certamente un incremento delle fratture, in particolare non vertebrali, e nei soggetti con DM2 trattati con insulina il rischio di caduta è di quattro volte più elevato rispetto a chi non assume questo farmaco.
Condizioni cliniche concomitanti
Anche se non si tratta di patologie, è giusto menzionare i cambiamenti fisiologici che avvengono nel corpo umano durante la gravidanza e l’allattamento, e come questi influiscano sull’apparato scheletrico. La gravidanza infatti è associata a un cambiamento della massa ossea e a un aumento della richiesta di calcio portando, talvolta, a un aumento del rischio di frattura.
Da non sottovalutare è l’osteoporosi associata all’allattamento(PLO), una condizione piuttosto grave di osteoporosi pre-menopausale che coinvolge la spina dorsale, che si può verificare nel terzo trimestre di gravidanza e durante l’allattamento. Per spiegare questo fenomeno possiamo partire da questo: un circuito cervello-mammella-ossa. L’allattamento e la prolattina (PRL) inibiscono entrambi il centro di rilascio dell’ormone ipotalamico delle gonadotropine (GnRH), che a sua volta sopprime le gonadotropine: ormone luteinizzante (LH) e ormone follicolo-stimolante (FSH), portando a bassi livelli di steroidi sessuali ovarici: estradiolo e progesterone. La prolattina può anche avere effetti diretti sul suo recettore nelle cellule ossee. La produzione e il rilascio di PTHrP dal seno sono stimolati dalla suzione, dalla prolattina, dall’estradiolo basso e dal recettore del calcio. Il PTHrP entra nel flusso sanguigno e si combina con livelli sistemicamente bassi di estradiolo portando a un aumento del riassorbimento osseo e (almeno nei roditori) l’osteolisi osteocitica. L’aumento del riassorbimento osseo rilascia calcio e fosfato nel flusso sanguigno, raggiungono i dotti mammari e vengono attivamente pompati nel latte materno. Oltre a stimolare l’espulsione del latte, l’ossitocina (OT) può influenzare direttamente la funzione degli osteoblasti e degli osteoclasti. Esistono diversi case reports che descrivono gli effetti positivi dei bisfosfonati su donne affette da osteoporosi associata all’allattamento, portando ad un aumento della BMD. Infine viene riportato il primo caso di paziente con questa tipologia di osteoporosi in trattamento con romosozumab, in seguito alla diagnosi di PLO per una bassa BMD e diverse fratture vertebrali nel primo mese post-parto; dopo 12 mesi di romosozumab la su BMD è aumentata del 23,6% per quanto riguarda le vertebre lombari, del 6,2% per il collo del femore e del 11,2% per il bacino.